醫療器械CRO以專業化優勢賦能產業高質量發展
- 2023-03-02 13:34
- 作者:郝帥
- 來源:弗若斯特沙利文
近年來,隨著國家相關支持性政策陸續發布以及資本助力,我國醫療器械行業蓬勃發展,醫療器械CRO行業也同時實現了快速發展。CRO作為連接醫療器械企業、醫療衛生機構等各方的重要橋梁,憑借眾多服務優勢,已然成為醫療器械產業鏈中的關鍵一環。
連接產業上下游
醫療器械CRO是連接醫療器械產業鏈上下游的重要橋梁,其上游包括醫療衛生機構、科學儀器廠商、實驗動物供應商等;下游主要是醫療器械企業。上游機構主要為醫療器械CRO提供臨床試驗數據、科學實驗儀器及實驗動物資源等;醫療器械CRO為下游醫療器械企業提供從臨床前研究、臨床試驗、注冊申報到上市后管理覆蓋全生命周期的專業化服務,以滿足醫療器械開發所特有的試驗需求和監管要求,幫助醫療器械企業縮短研發周期,降低研發成本及研發風險,為推動醫療器械產品成功上市、規范上市后管理提供助力。
醫療機構:醫療器械臨床試驗機構規范化、專業化管理,為醫療器械CRO行業發展創造良好環境
2017年11月,《醫療器械臨床試驗機構條件和備案管理辦法》(以下簡稱《管理辦法》)正式發布。根據《管理辦法》,對符合醫療器械臨床試驗質量管理規范要求且具備開展臨床試驗能力的醫療器械臨床試驗機構,實行備案管理。自2018年《管理辦法》實施以來,醫療器械臨床試驗機構備案數量持續增長。根據國家藥監局統計數據,截至目前,共有1236個臨床機構完成備案。作為醫療器械CRO的上游環節,專業化、規范化的臨床試驗機構將持續提高醫療器械臨床試驗質量,為醫療器械CRO行業發展創造良好環境。
醫療器械CRO:目前我國醫療器械CRO行業集中度較低,多以中小型企業為主
我國醫療器械CRO行業起步較晚,企業數量眾多,以中小型企業為主,市場集中度較低。由于醫療器械CRO行業基礎服務準入門檻較低,多數企業的業務范圍主要集中于提供臨床試驗服務、注冊申報服務等。在下游市場需求及國家政策的推動下,我國醫療器械CRO企業的服務范圍和服務領域將持續拓展,逐漸覆蓋醫療器械研發檢測、動物試驗、臨床試驗、注冊申報、上市后管理全生命周期,同時行業將實現加速整合,市場持續擴容。
醫療器械企業:我國醫療器械生產企業數量逐年遞增,行業實現穩步發展
國家藥監局統計數據顯示,截至2020年底,全國共有2.65萬家醫療器械生產企業,較2017年增長18.3%;可生產第二、三類醫療器械的企業數量分別為1.30萬家、2181家,呈逐年遞增趨勢,醫療器械行業整體實現穩步發展。作為醫療器械CRO的下游,醫療器械生產企業數量的增加,進一步催生了對醫療器械CRO的需求。
服務全生命周期
依據國家藥監局和國家衛生健康委于2022年3月發布的《醫療器械臨床試驗質量管理規范》,在醫療器械臨床試驗開始前,申辦者應當通過主要研究者向倫理委員會提交基于產品技術要求的產品檢驗報告。
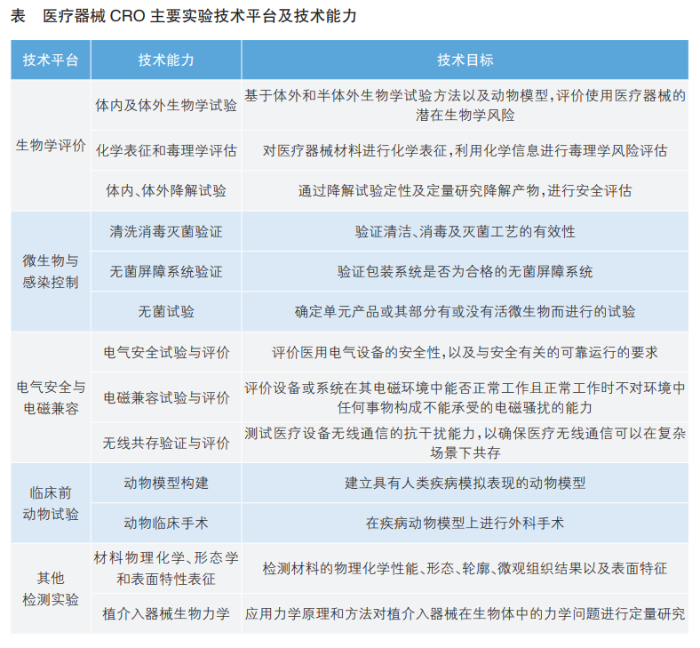
醫療器械CRO通過整合實驗室資源,搭建包括生物學評價、微生物與感染控制、電氣安全與電磁兼容、臨床前動物試驗等在內的多個實驗技術平臺,建設相關技術能力,可充分滿足醫療器械檢驗檢測需求(詳見表)。
目前,體外診斷試劑相關服務是醫療器械CRO企業積極拓展的新興業務領域。
我國醫療器械按風險程度實行分類管理,不同類別的醫療器械產品分別通過備案管理或注冊管理實現有效控制。醫療器械CRO可依據醫療器械企業產品分類,提供定制化服務內容。
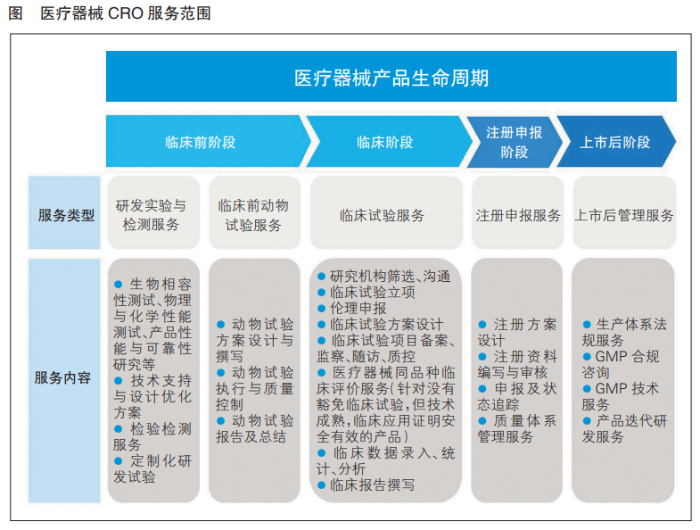
醫療器械CRO服務范圍廣泛,主要包括臨床前的研發檢測服務、動物試驗服務,臨床試驗服務,注冊申報服務,上市后的生產體系法規服務及產品迭代研發服務等,服務內容覆蓋醫療器械全生命周期(詳見圖)。
在我國醫療器械CRO行業發展初期,多數CRO企業主要提供臨床組合服務及注冊申報服務。隨著醫療器械行業快速發展,行業監管日趨嚴格和完善,醫療器械企業需求發生變化,從而推動專注于醫療器械生命周期其他階段業務的醫療器械CRO企業不斷涌現,其服務內容更加專業和細化,服務類型包括臨床前階段的研發試驗與檢測、動物試驗等。
助力創新成果轉化
醫療器械CRO作為專門服務于醫療器械領域的第三方外包組織,具有眾多服務優勢:擁有專業化且經驗豐富的團隊及規模化平臺,可提供全生命周期服務,并通過與創新鏈各主體深度合作加快創新資源布局,有效幫助醫療器械企業縮短產品研發及上市周期,協助企業驗證產品的安全性及有效性,降低研發風險和研發成本,助力醫療器械企業實現創新成果轉化。
醫療器械CRO的專業化團隊高度契合醫療器械產業發展特點,可幫助企業解決產品研發上市過程中的潛在問題
醫療器械產業是一個多學科交叉、多知識密集、多領域細分的高技術產業。多學科交叉體現在涉及生命科學、臨床醫學、電子科技、信息工程、材料科學等多個學科;多知識密集體現在醫療器械從研發到上市銷售過程涉及設計開發、專利產權、法律法規、工藝開發、生產管理等多門類知識;多領域細分體現在醫療器械可依據用途劃分為骨科器械、眼科器械、醫療影像設備、重癥監護設備等。
醫療器械CRO擁有專業化團隊,聚集了不同學科背景的專業人才,他們掌握醫療器械全生命周期涉及的各種專業知識,并且在不同醫療器械細分領域積累了豐富經驗,高度契合醫療器械產業發展特點,可有效幫助醫療器械企業解決產品研發上市過程中的各種問題。
醫療器械CRO深植醫療器械領域,可提供全生命周期服務,幫助醫療器械企業降低失敗風險
醫療器械的成功上市,需要經過產品設計研發、質量體系建立、檢驗檢測、臨床試驗、注冊申報、生產體系建立等階段,過程漫長、失敗風險高且投資巨大。醫療器械CRO作為專門為醫療器械企業提供專業化服務的第三方組織,深植醫療器械領域,服務范圍覆蓋醫療器械全生命周期。其通過整合優質資源,可很大程度上幫助醫療器械企業在產品研發過程中實現高質量研究和低成本投入,很好滿足企業風險控制的需求,同時推動創新成果快速轉化。
醫療器械CRO整合企業試驗需求,規模化建設綜合平臺,相比企業自建實驗平臺更加高效
醫療器械關系人民群眾身體健康和生命安全。醫療器械產品在開展臨床試驗前必須通過多種檢測項目來評價其安全性及有效性,包括EMC電磁兼容檢測、電氣安全檢測、生物相容性檢測、微生物檢測、包裝材料檢測等。不同的檢測項目包括多項試驗內容,如生物相容性檢測可分為細胞毒性試驗、刺激和致敏試驗、全身毒性試驗、植入試驗、遺傳毒性試驗、發育毒性試驗、血液相容性試驗、生物降解試驗等。不同試驗對實驗室及實驗儀器設備的要求不盡相同。企業自建實驗平臺需要打造專門的試驗團隊,搭建一定規模的實驗室,并配備相應的儀器設備,投入成本較高,且較難滿足全部的試驗需求。而醫療器械CRO通過建設規模化的綜合實驗平臺,可整合醫療器械企業試驗需求,充分利用實驗室資源,相比于企業自建實驗平臺進行檢測的模式更加高效。
醫療器械CRO為產業鏈的關鍵環節,深度融合創新鏈,加快創新資源布局,打造高科技創新閉環
創新鏈是指以某創新主體為核心,多主體協同配合,以滿足市場需求為導向,從基礎研究到產業化的創新過程的集合。創新主體構成復雜,包括企業、科研機構、高校、投資機構、政府、中介機構、推廣機構、產業園區等。
醫療器械CRO作為醫療器械產業鏈的關鍵環節,深度融合創新鏈,通過與醫療器械企業、行業協會、臨床醫療機構、高校、產業園區等進行合作,形成以政府宏觀調控為導向,以政策制度為激勵,以醫療器械CRO為橋梁,以高校、科研院所、科技金融服務機構為支撐的運行機制,推動產學研協同創新,加速創新資源布局,打造高科技創新閉環,幫助醫療器械企業進行創新成果轉化。
未來,在醫療器械領域利好政策和市場需求的共同推動下,醫療器械CRO行業集中度將進一步提高,服務范圍與服務領域將持續拓展,實現對醫療器械全生命周期的覆蓋。(作者單位:弗若斯特沙利文)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:申楊)
右鍵點擊另存二維碼!
-
為你推薦
互聯網新聞信息服務許可證10120170033
網絡出版服務許可證(京)字082號
?京公網安備 11010802023089號 京ICP備17013160號-1
《中國醫藥報》社有限公司 中國食品藥品網版權所有