2月份美國Clinicaltrial數據庫臨床試驗數據顯示——我國三家企業進入新開臨床試驗數量排名前十
- 2025-04-03 09:29
- 作者:陳宇哲
- 來源:中國醫藥報
根據美國Clinicaltrial數據庫數據,2025年2月份,全球新增由企業資本主導的臨床試驗總數為652項,新開臨床試驗數量較1月份下降7.52%。單月新增臨床試驗數量顯著高于去年同期水平,上升19.85%。值得注意的是,我國有3家企業進入新開臨床試驗數量排名前十,分別為山東盛迪醫藥、神州細胞和微康益生菌。
新開臨床試驗整體情況
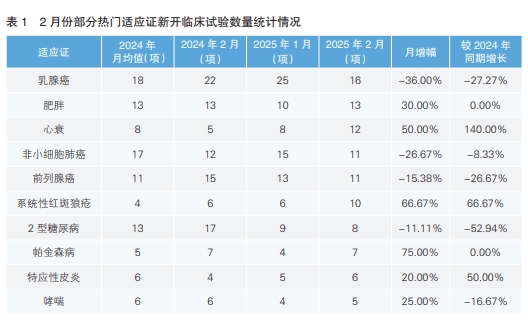
從2月份新增臨床試驗熱門適應證領域來看,乳腺癌為最熱門的研發領域,試驗數量為16項,環比下降36.00%,相較于去年同期數量下降27.27%。其次為肥胖,新開臨床試驗數量環比上升30.00%,與去年同期數量持平。值得注意的是,2月份新增臨床試驗數量上升幅度最高的熱門適應證為帕金森病,由1月份的4項上升為7項,上升幅度為75%。除此之外,相較于去年同期,上升幅度最大的適應證為心衰,由5項上升為12項,增幅為140%。(詳見表1)
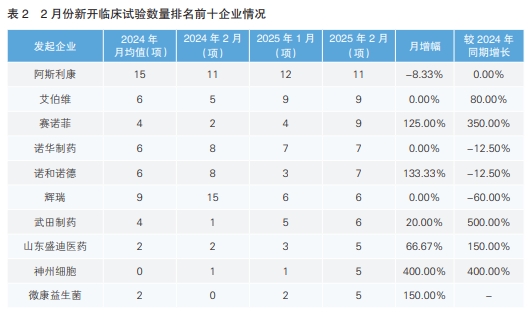
對新增臨床試驗的發起企業進行統計后發現,2月份發起臨床試驗最多的企業為阿斯利康,數量相較于1月份下降了8.33%,但與去年同期持平。其次為艾伯維,數量與1月份持平,較去年同期增長80.00%。與1月份相比,新增臨床試驗數量增幅最大的企業為我國的神州細胞,環比上升了4倍。相較于去年同期,數量上升幅度最大的為武田制藥,上漲了5倍。(詳見表2)
對臨床試驗的申請國家和地區進行統計后發現,2月份美國仍為臨床試驗開展最為主要的國家,新開展臨床試驗218項,數量環比下降了1.80%。其次是中國,新開設臨床試驗數量為80項,數量環比上升了1.27%。2月份新開臨床試驗數量月增長幅度最大的國家為荷蘭,由6項增長為7項,增長幅度為16.67%。
我國三家企業新增5項臨床試驗
2月份,我國的山東盛迪醫藥、神州細胞和微康益生菌均進入新開臨床試驗數量排名前十的企業榜單。這3家企業新開設臨床試驗均為5項。
山東盛迪醫藥2月份新增臨床試驗包括3項Ⅱ期臨床試驗和兩項Ⅰ期臨床試驗。
3項Ⅱ期臨床試驗的藥物分別為HRS-7535(NCT06820099),適應證為成人肥胖伴心力衰竭伴射血分數保留;HRS-5346(NCT06816264),適應證為脂蛋白紊亂的治療;HRS-1893(NCT06816251),適應證為非梗阻性肥厚型心肌病。
公開數據顯示,HRS-7535是一種新型口服小分子GLP-1RA。臨床前研究發現,在無嚴格限食的情況下,HRS-7535可明顯改善葡萄糖耐量,促進胰島素分泌,減少攝食量。HRS-5346是一種口服小分子脂蛋白(a)[也稱Lp(a)]抑制劑。Lp(a)是一類獨特的脂蛋白,含有低密度脂蛋白樣顆粒,具有促動脈粥樣硬化、促炎、促鈣化等作用。高Lp(a)是動脈粥樣硬化性心血管疾病的獨立危險因素,也是主動脈瓣狹窄的危險因素。因此,靶向Lp(a)的降脂療法是心血管疾病防治的重要突破點之一。HRS-1893可通過特殊機制抑制心肌過度收縮。據悉,該藥是國內第一個使用心臟器官芯片數據獲批I ND的新藥。
兩項Ⅰ期臨床試驗的藥品分別為[14C] HRS-7535(NCT06819488),適應證為2型糖尿病;HRS-2129(NCT06780267),適應證為骨科術后疼痛。
神州細胞新增的5項臨床試驗均處于Ⅰ/Ⅱ期臨床試驗階段,其中兩項為藥品,兩項為疫苗,一項為生物療法。
兩款藥物分別為SCTT11(NCT06769984)適應證為甲狀腺眼病,以及SCT520FF(NCT06672536),適應證為新生血管性黃斑變性。公開資料顯示,這兩款藥品均為單克隆抗體。兩款疫苗中,SCTV04C(NCT06801509)的適應證為帶狀皰疹;另一款疫苗SCTV02(NCT06754605),適應證為呼吸道合胞病毒。生物療法為SCTB35(NCT06841042),適應證為系統性紅斑狼瘡。根據公開資料,SCTB35是神州細胞開發的CD20/CD3雙抗。
微康益生菌的5項臨床試驗,試驗對象均為膳食補充劑。
(數據來源于美國Clinicaltrial數據庫,統計時間為2025年3月5日)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:張可欣)
右鍵點擊另存二維碼!
-
為你推薦