《中國藥典》2020年版第四部藥用輔料和藥包材
- 2020-09-15 15:40
- 作者:
- 來源:《中國藥品標(biāo)準(zhǔn)》雜志
《中華人民共和國藥典》(簡稱《中國藥典》)是藥品生產(chǎn)、流通、使用和監(jiān)管所必須遵循的法定技術(shù)要求,其中不僅包括中藥、化學(xué)藥和生物制品等藥品標(biāo)準(zhǔn),藥用輔料和藥包材標(biāo)準(zhǔn)也是其中不可或缺的重要組成部分。近年來隨著仿制藥質(zhì)量與療效一致性評價(jià)工作的深入推進(jìn),藥品生產(chǎn)企業(yè)和監(jiān)管部門越發(fā)意識到藥用輔料和藥包材的標(biāo)準(zhǔn)在藥品評價(jià)和質(zhì)控方面的重要作用。秉承制定“最嚴(yán)謹(jǐn)?shù)臉?biāo)準(zhǔn)”的工作理念,按照《中國藥典2020年版編制大綱》確定的工作目標(biāo)和任務(wù),在國家藥品監(jiān)管部門的指導(dǎo)下,國家藥典委員會(huì)精心組織30余家標(biāo)準(zhǔn)提高課題承擔(dān)單位深入研究,并經(jīng)第十一屆國家藥典委員會(huì)藥用輔料與藥包材專業(yè)委員會(huì)全體委員和特邀專家的認(rèn)真審核,現(xiàn)已完成2020年版《中國藥典》(以下簡稱“本版藥典”)藥用輔料和藥包材標(biāo)準(zhǔn)的制定和修訂工作。
本版藥典中的藥用輔料和藥包材標(biāo)準(zhǔn)與通用技術(shù)要求部分一并收載于《中國藥典》的第四部,其標(biāo)準(zhǔn)既與《中國藥典》渾然一體,又獨(dú)具特色。為使《中國藥典》的使用者正確理解、執(zhí)行或運(yùn)用相關(guān)標(biāo)準(zhǔn),本文著重介紹了本版藥典中藥用輔料和藥包材標(biāo)準(zhǔn)體系的總體框架和主要特點(diǎn)。
1 《中國藥典》藥用輔料和藥包材標(biāo)準(zhǔn)的歷史沿革
1.1 藥用輔料標(biāo)準(zhǔn)
1.1.1 我國藥用輔料標(biāo)準(zhǔn)概況
我國上市藥品所執(zhí)行的藥用輔料標(biāo)準(zhǔn)比較多元化,既包括《中國藥典》和國外藥典,也包括執(zhí)行注冊審批制時(shí)產(chǎn)生的國家標(biāo)準(zhǔn)、局部頒標(biāo)準(zhǔn)、地方標(biāo)準(zhǔn)等,還有正在執(zhí)行的化工標(biāo)準(zhǔn)、食品級產(chǎn)品標(biāo)準(zhǔn)以及企業(yè)內(nèi)控標(biāo)準(zhǔn)等。
1.1.2 《中國藥典》藥用輔料標(biāo)準(zhǔn)的收載情況
《中國藥典》中收載藥用輔料品種正文的形式可大體分為三個(gè)階段。第一階段:從第一版《中國藥典》(1953年版)開始,就收載了蒸餾水、鹽酸、醋酸、硝酸、硫酸、濃氨溶液、蔗糖、淀粉、硬脂酸等藥用輔料標(biāo)準(zhǔn),這既體現(xiàn)了藥用輔料標(biāo)準(zhǔn)對于藥品質(zhì)量控制的重要性,也充分說明了《中國藥典》對于藥用輔料高度關(guān)注由來已久。從第二版(1963年版)起,《中國藥典》分為一部(中藥)和二部(化藥為主)兩部,藥用輔料標(biāo)準(zhǔn)被納入二部藥典,與其他品種混合編排,此種方式一直延續(xù)到2005年版。
第二階段:從2005年版《中國藥典》開始,藥用輔料改為在二部中單獨(dú)列出,稱為“正文品種 第二部分”,更便于檢索查閱;該版藥典共收載73個(gè)藥用輔料標(biāo)準(zhǔn)。2010年版《中國藥典》新增62個(gè)藥用輔料標(biāo)準(zhǔn),總數(shù)擴(kuò)增到132個(gè);該版還首次收載了藥用輔料的通則(附錄II),擴(kuò)充了藥用輔料的藥典標(biāo)準(zhǔn)體系。
第三階段:自2015年版《中國藥典》,藥用輔料標(biāo)準(zhǔn)與通則類標(biāo)準(zhǔn)合并單獨(dú)形成了《中國藥典》第四部,新增138個(gè)藥用輔料標(biāo)準(zhǔn),總數(shù)擴(kuò)增到270個(gè);并首次收載了9601<藥用輔料功能性指標(biāo)研究指導(dǎo)原則>,強(qiáng)化了藥用輔料功能性相關(guān)指標(biāo)在標(biāo)準(zhǔn)體系中的地位[1]。本版藥典繼續(xù)擴(kuò)大藥用輔料品種標(biāo)準(zhǔn)的收載,新增65個(gè),修訂212個(gè)(有實(shí)質(zhì)修訂的116個(gè),僅文字規(guī)范的96個(gè));新增藥用輔料指導(dǎo)原則2個(gè),修訂藥用輔料通則和指導(dǎo)原則各1個(gè)。所列數(shù)據(jù)表明,本版藥典的藥用輔料標(biāo)準(zhǔn)體系更加完備。
1.2 藥包材標(biāo)準(zhǔn)
1.2.1 我國藥包材標(biāo)準(zhǔn)概況
我國現(xiàn)行的藥包材標(biāo)準(zhǔn)比較多元化,既包括《中國藥典》和國外藥典,也包括2015年版《國家藥包材標(biāo)準(zhǔn)》、執(zhí)行注冊審批制時(shí)產(chǎn)生的國家標(biāo)準(zhǔn)和企業(yè)內(nèi)控標(biāo)準(zhǔn)等。
1.2.2 《中國藥典》藥包材標(biāo)準(zhǔn)的收載情況
在2015年版《中國藥典》(第十版)中首次收載了9621<藥包材通用要求指導(dǎo)原則>和9622<藥用玻璃材料和容器指導(dǎo)原則>兩個(gè)指導(dǎo)原則,開啟了藥包材標(biāo)準(zhǔn)納入《中國藥典》的序幕,也強(qiáng)化了對藥包材及其重要門類玻璃材料的總體要求。
基于對藥包材標(biāo)準(zhǔn)體系的進(jìn)一步研究,按照“總體規(guī)劃,分步推進(jìn)”的原則,在本版藥典中加強(qiáng)了藥包材通用檢測方法的收載,新增通用檢測方法16個(gè),進(jìn)一步擴(kuò)充了藥典藥包材標(biāo)準(zhǔn)體系,為后續(xù)藥包材標(biāo)準(zhǔn)體系的整體完善奠定了基礎(chǔ)。
2 本版藥典藥用輔料和藥包材的標(biāo)準(zhǔn)體系
2.1 藥用輔料的標(biāo)準(zhǔn)體系
2.1.1 三位一體結(jié)構(gòu)更加清晰
本版藥典藥用輔料標(biāo)準(zhǔn)由品種正文及其引用的凡例、通用技術(shù)要求共同構(gòu)成。在藥典編制中特別注重了四部凡例、相關(guān)通用技術(shù)要求與各品種正文的銜接,做到三者“各司其職”。凡例是為正確使用《中國藥典》進(jìn)行質(zhì)量檢驗(yàn)和檢定的基本原則,故將上版四部凡例中藥用輔料應(yīng)符合GMP及單獨(dú)審批等已與現(xiàn)行的原輔包關(guān)聯(lián)審評審批制度不符的內(nèi)容刪去,以便與現(xiàn)行管理制度及法規(guī)相匹配。將上版四部凡例二十二條中關(guān)于藥用輔料生產(chǎn)和使用的具體規(guī)定歸入通則0251<藥用輔料>中,以使四部凡例內(nèi)容更聚焦于藥用輔料質(zhì)量檢驗(yàn)和檢定的共性問題。在本版藥典四部凡例的正文內(nèi)容、名稱與編排、來源與制法、檢查項(xiàng)、含量測定項(xiàng)、含量限度范圍、類別等章節(jié)突出了藥用輔料的特點(diǎn)。作為《中國藥典》四部的總綱和說明,本版藥典四部凡例中明確規(guī)定“制劑生產(chǎn)使用的藥用輔料,應(yīng)符合相關(guān)法律、法規(guī)、部門規(guī)章和規(guī)范性文件,以及本版藥典通則0251<藥用輔料>的有關(guān)要求”,由此確定了通則0251的強(qiáng)制執(zhí)行性。
通用技術(shù)要求包括《中國藥典》收載的通則、指導(dǎo)原則等;通則主要包括制劑通則、其他通則、通用檢測方法。指導(dǎo)原則系為規(guī)范藥典執(zhí)行,指導(dǎo)藥品標(biāo)準(zhǔn)制定和修訂,提高藥品質(zhì)量控制水平所規(guī)定的非強(qiáng)制性、推薦性技術(shù)要求。本版藥典收載的藥用輔料通用技術(shù)要求包括通則0251<藥用輔料>,9601<藥用輔料功能性相關(guān)指標(biāo)指導(dǎo)原則>(修訂)、9602<動(dòng)物源藥用輔料指導(dǎo)原則>(新增)和9603<預(yù)混與共處理藥用輔料質(zhì)量控制指導(dǎo)原則>(新增)3個(gè)指導(dǎo)原則以及相關(guān)的通用檢測方法。本版藥典藥用輔料通用技術(shù)要求結(jié)構(gòu)圖見圖1。
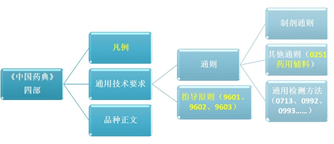
圖1 2020年版《中國藥典》藥用輔料通用技術(shù)要求結(jié)構(gòu)圖
Fig.1 The structure chart on general technical requirements of pharmaceutical excipients in 2020 edition of Chinese Pharmacopoeia
2.1.2 藥用輔料通則強(qiáng)化藥典藥用輔料標(biāo)準(zhǔn)定位
根據(jù)原輔包與制劑關(guān)聯(lián)審評審批的制度導(dǎo)向,本版藥典通則0251<藥用輔料>中特別強(qiáng)調(diào)了在藥品制劑研發(fā)和上市后變更研究中,對藥用輔料的選用應(yīng)以制劑質(zhì)量為中心,以滿足制劑的質(zhì)量要求和設(shè)計(jì)目標(biāo)為依據(jù),加強(qiáng)藥用輔料的適用性研究。適用性研究應(yīng)充分考慮藥用輔料的來源、工藝,及其制備制劑的特點(diǎn)、給藥途徑、使用人群和使用劑量等相關(guān)因素的影響。
基于上述理念,本版藥典通則0251<藥用輔料>中特別說明了《中國藥典》藥用輔料標(biāo)準(zhǔn)的定位。①權(quán)威性。《中華人民共和國藥品管理法》第二十八條規(guī)定:國務(wù)院藥品監(jiān)督管理部門頒布的《中華人民共和國藥典》和藥品標(biāo)準(zhǔn)為國家藥品標(biāo)準(zhǔn)。《國家藥監(jiān)局關(guān)于進(jìn)一步完善藥品關(guān)聯(lián)審評審批和監(jiān)管工作有關(guān)事宜的公告》(2019年第56號)等管理文件中也將《中國藥典》的藥用輔料標(biāo)準(zhǔn)列為重要參考標(biāo)準(zhǔn)。作為《中國藥典》的重要組成部分之一的藥用輔料標(biāo)準(zhǔn)已經(jīng)成為藥用輔料生產(chǎn)、選用、審評審批及監(jiān)管的重要依據(jù)。通則0251中也指出了“《中國藥典》收載的藥用輔料標(biāo)準(zhǔn)是對其質(zhì)量控制的基本標(biāo)準(zhǔn)”。②首選性。通則0251中規(guī)定:對于聲稱符合《中國藥典》的藥用輔料必須執(zhí)行《中國藥典》的相應(yīng)標(biāo)準(zhǔn)正文。如經(jīng)研究確認(rèn)《中國藥典》收載的藥用輔料標(biāo)準(zhǔn)不能全部適用于某一藥品的安全性、有效性及制劑的需求,或《中國藥典》尚未收載某藥用輔料品種或規(guī)格,在藥品制劑研發(fā)和上市后變更研究中可選擇適宜的藥用輔料,并制定相應(yīng)的內(nèi)控標(biāo)準(zhǔn)。從而突出了藥典藥用輔料標(biāo)準(zhǔn)的強(qiáng)制首選性和適用性研究的必要性。③與時(shí)俱進(jìn)性。通則0251中規(guī)定:《中國藥典》收載的藥用輔料標(biāo)準(zhǔn)應(yīng)根據(jù)已上市藥品中使用的藥用輔料的質(zhì)量特點(diǎn),在充分評估的基礎(chǔ)上,適時(shí)進(jìn)行修訂。著重強(qiáng)調(diào)了藥典藥用輔料標(biāo)準(zhǔn)應(yīng)結(jié)合實(shí)際應(yīng)用和產(chǎn)品技術(shù)更新而不斷完善,著重挖掘藥用輔料的關(guān)鍵質(zhì)量屬性,并以適宜的方式體現(xiàn)在《中國藥典》這個(gè)載體中。
2.1.3 構(gòu)建藥用輔料功能性相關(guān)指標(biāo)的標(biāo)準(zhǔn)體系
藥品的關(guān)鍵質(zhì)量屬性可以分為安全性、有效性和質(zhì)量均一性,而藥用輔料除了安全性和質(zhì)量均一性至關(guān)重要外,其有效性不體現(xiàn)在功能主治和療效用途方面,而是體現(xiàn)在其在制劑中發(fā)揮的功能性方面。根據(jù)藥用輔料在制劑中發(fā)揮的功能,其可分為稀釋劑、黏合劑等數(shù)十種,每種功能有不同的功能性相關(guān)指標(biāo)來體現(xiàn)或區(qū)分,這些指標(biāo)又需要有一定通用性和標(biāo)準(zhǔn)化的檢測方法來評價(jià),以便使其更好的體現(xiàn)在有強(qiáng)制性的標(biāo)準(zhǔn)中。各國藥典對藥用輔料的功能性相關(guān)指標(biāo)規(guī)范程度、表述體例等均不相同,研究建立《中國藥典》藥用輔料功能性相關(guān)指標(biāo)標(biāo)準(zhǔn)體系對藥用輔料質(zhì)量控制至關(guān)重要,亦可推動(dòng)藥用輔料產(chǎn)業(yè)升級、推進(jìn)國產(chǎn)制劑質(zhì)量療效提升。本版藥典在編制過程中,結(jié)合行業(yè)發(fā)展階段的特點(diǎn)和《中國藥典》在監(jiān)管中的地位和作用,構(gòu)建了適宜的藥用輔料功能性相關(guān)指標(biāo)標(biāo)準(zhǔn)體系,包括以下4個(gè)層級:
①細(xì)化分類指導(dǎo)原則。本版藥典修訂了指導(dǎo)原則9601,該指導(dǎo)原則在《中國藥典》2015年版首次收載,原名<藥用輔料功能性研究指導(dǎo)原則>,介紹了藥用輔料11類功能的功能性指標(biāo)。本版藥典對其名稱進(jìn)行了規(guī)范,將原“功能性指標(biāo)”統(tǒng)一改為“功能性相關(guān)指標(biāo)”,使表述更為貼切;功能類別擴(kuò)展為19類;每一類中分概述、化學(xué)性質(zhì)、物理性質(zhì)、功能機(jī)制、功能性相關(guān)指標(biāo)幾部分進(jìn)行詳細(xì)闡述;《中國藥典》中已有通用檢測方法的,均在每個(gè)功能性相關(guān)指標(biāo)后加注了相應(yīng)通則或指導(dǎo)原則的編號。
②增訂通用檢測方法。鑒于功能性相關(guān)指標(biāo)的通用檢測方法對于評價(jià)藥用輔料功能性至關(guān)重要,國家藥典委員會(huì)一直在致力于組織相關(guān)單位對其進(jìn)行研究開發(fā)。本版藥典新增了相關(guān)的通用檢測方法0992<固體密度>和0993<堆密度與振實(shí)密度>,后續(xù)將逐步把成熟的方法納入《中國藥典》。
③擬定編寫指導(dǎo)原則。藥用輔料功能性相關(guān)指標(biāo)的評價(jià)在《中國藥典》標(biāo)準(zhǔn)中主要是通過【檢查】項(xiàng)和【標(biāo)示】項(xiàng)體現(xiàn)。【檢查】項(xiàng)通常屬于必檢項(xiàng)目;【標(biāo)示】項(xiàng)屬于必標(biāo)示項(xiàng)目。本版藥典通則0251中規(guī)定“本部正文標(biāo)示項(xiàng)下規(guī)定應(yīng)標(biāo)明的內(nèi)容應(yīng)在產(chǎn)品標(biāo)簽、包裝、質(zhì)量標(biāo)準(zhǔn)或檢驗(yàn)報(bào)告書(其中至少一個(gè))中標(biāo)明”,以便藥用輔料的使用方和監(jiān)管方進(jìn)行識別、檢驗(yàn)及監(jiān)管;另外還規(guī)定“僅在標(biāo)示項(xiàng)中涉及的功能性相關(guān)指標(biāo),其檢測方法及限度要求應(yīng)由藥用輔料供需方在檢驗(yàn)報(bào)告書或質(zhì)量協(xié)議等載體中載明”,以便完善功能性相關(guān)指標(biāo)標(biāo)準(zhǔn)體系并使其更具可操作性。
④拓展品種正文功能性相關(guān)指標(biāo)收載。如硅酸鎂鋁修訂了標(biāo)準(zhǔn)中的來源描述,從源頭上保證其功能性的要求。又如十二烷基硫酸鈉在【檢查】項(xiàng)中增訂了脂肪醇組成項(xiàng),并在【標(biāo)示】項(xiàng)規(guī)定“應(yīng)標(biāo)明十二醇的標(biāo)示值,以及十二醇與十四醇的含量之和的標(biāo)示值”。此標(biāo)準(zhǔn)表述方式既可控制一家企業(yè)生產(chǎn)的十二烷基硫酸鈉的批間差異,也可區(qū)分不同企業(yè)生產(chǎn)的十二烷基硫酸鈉之間組分的差異。又如本版藥典通過【標(biāo)示】項(xiàng),新增了對部分藥用輔料功能性相關(guān)指標(biāo)的要求,如膠態(tài)二氧化硅增加標(biāo)示比表面積;微晶纖維素增加標(biāo)示產(chǎn)品型號、粒度分布、堆密度;白陶土增加標(biāo)示吸著力和膨脹力等。
本版藥典通過構(gòu)建藥用輔料功能性相關(guān)指標(biāo)標(biāo)準(zhǔn)體系,使《中國藥典》藥用輔料標(biāo)準(zhǔn)更好體現(xiàn)藥用輔料特性、控制藥用輔料質(zhì)量,強(qiáng)化了《中國藥典》的指導(dǎo)性和可操作性,推動(dòng)藥用輔料功能性相關(guān)指標(biāo)的深入研究,更好為仿制藥一致性評價(jià)及關(guān)聯(lián)審評審批提供技術(shù)支撐。
2.2 藥包材的標(biāo)準(zhǔn)體系
目前,影響較大的國外藥典標(biāo)準(zhǔn)體系,如美國藥典(USP)、歐洲藥典(EP)、日本藥局方(JP)等,均已收載相關(guān)藥包材標(biāo)準(zhǔn)。從其藥典標(biāo)準(zhǔn)框架體系來看,其藥包材系列標(biāo)準(zhǔn)更加側(cè)重于以材料及其容器為主線的通用性標(biāo)準(zhǔn),如玻璃、塑料、橡膠材料和/或其成品的通用要求。同時(shí)涵蓋了滿足通用要求評價(jià)的性能測試方法。除此之外,USP還設(shè)立了更為廣泛的評價(jià)和研究指南性章節(jié)。在此基礎(chǔ)上的標(biāo)準(zhǔn)框架體系將更加有利于具體藥包材產(chǎn)品的標(biāo)準(zhǔn)制定。
我國藥典藥包材標(biāo)準(zhǔn)還在起步階段,為了構(gòu)建更加合理、完善的中國藥典藥包材標(biāo)準(zhǔn)體系,國家藥典委員會(huì)特別設(shè)立專項(xiàng)課題“藥包材標(biāo)準(zhǔn)體系規(guī)劃和體例規(guī)范”進(jìn)行研究。基于“借鑒國內(nèi)外經(jīng)驗(yàn),立足我國國情,國家標(biāo)準(zhǔn)保基本”的總原則,初步確定《中國藥典》藥包材標(biāo)準(zhǔn)體系建立的思路為:
①關(guān)注基本要求:建立藥包材生產(chǎn)使用的基本要求(通則或指導(dǎo)原則),規(guī)定各類藥包材的安全性及其它必須的通用性基本要求。
②關(guān)注安全性評價(jià):結(jié)合關(guān)聯(lián)審評審批的需要,適時(shí)完善藥包材安全性評價(jià)指導(dǎo)原則等。
③關(guān)注功能性評價(jià):通過建立包括阻隔性能、密封性能、自身穩(wěn)定性和使用性能等關(guān)鍵項(xiàng)目的檢測方法,為確保產(chǎn)品功能性奠定基礎(chǔ)。
④關(guān)注對個(gè)性化產(chǎn)品標(biāo)準(zhǔn)的指導(dǎo):對某類藥包材生產(chǎn)和質(zhì)量控制制定基本的通用的技術(shù)要求,指導(dǎo)行業(yè)和企業(yè)制定個(gè)性化的產(chǎn)品標(biāo)準(zhǔn)。如腹透包裝系統(tǒng)、吸入制劑包裝系統(tǒng)等,各企業(yè)各產(chǎn)品有特定的一些指標(biāo)和參數(shù),個(gè)性化、定制化、保密性的特點(diǎn)較突出,不宜制定單一的、公開的且強(qiáng)制的產(chǎn)品標(biāo)準(zhǔn),可通過對該類產(chǎn)品的通用技術(shù)要求,指導(dǎo)企業(yè)根據(jù)基本要求制定完善合理的產(chǎn)品標(biāo)準(zhǔn)。
結(jié)合藥典編制大綱的要求和原則,根據(jù)現(xiàn)有藥典標(biāo)準(zhǔn)“以凡例為總體要求、通用技術(shù)要求為基本規(guī)定、正文為具體要求”的特點(diǎn),故本版藥典首次收載了目前應(yīng)用比較廣泛、較成熟的16個(gè)通用檢測方法,后續(xù)將把成熟的相關(guān)通用技術(shù)要求和通用檢測方法逐步收載入藥典。
3 本版藥典藥用輔料和藥包材通用技術(shù)要求的主要特點(diǎn)
3.1 加強(qiáng)特殊藥用輔料全鏈條質(zhì)量管理
為加強(qiáng)對動(dòng)物來源輔料、預(yù)混和共處理輔料的全鏈條質(zhì)量管理及風(fēng)險(xiǎn)防控,本版藥典首次收載了9602<動(dòng)物源藥用輔料指導(dǎo)原則>和9603<預(yù)混與共處理藥用輔料質(zhì)量控制指導(dǎo)原則>兩個(gè)指導(dǎo)原則,均填補(bǔ)了《中國藥典》該領(lǐng)域技術(shù)要求的空白。
9602<動(dòng)物源藥用輔料指導(dǎo)原則>在概述部分明確了所謂動(dòng)物來源藥用輔料的定義和分類,闡明了該指導(dǎo)原則的適用范圍。后續(xù)分原材料的一般要求(包括入選標(biāo)準(zhǔn)、來源、批次、質(zhì)控要求等)、生產(chǎn)工藝和過程控制(包括生產(chǎn)工藝研究、外源因子的滅活/去除等)、質(zhì)量研究和穩(wěn)定性研究(包括基于原材料特點(diǎn)和制劑特性的質(zhì)量研究、穩(wěn)定性研究與貯藏要求等)和供應(yīng)商審計(jì)(對輔料供應(yīng)商的審計(jì)、對輔料原材料供應(yīng)商的審計(jì)等)詳述了該類藥用輔料的質(zhì)控關(guān)鍵點(diǎn)及注意事項(xiàng)。
9603<預(yù)混與共處理藥用輔料質(zhì)量控制指導(dǎo)原則>全面梳理了預(yù)混輔料和共處理輔料這兩類加工較為特殊的藥用輔料,其在生產(chǎn)過程管理和質(zhì)量標(biāo)準(zhǔn)建立方面的關(guān)鍵點(diǎn),包括概述(定義、分類、適用范圍等)、生產(chǎn)工藝和過程控制、質(zhì)量控制(性狀、鑒別、檢查、功能性指標(biāo)、含量及功能有效性指標(biāo)、微生物限度、穩(wěn)定性研究)等內(nèi)容。
3.2 加強(qiáng)藥包材通用檢測方法的規(guī)范
3.2.1 玻璃容器相關(guān)測試方法
4001<121 ℃玻璃顆粒耐水性測定法>明確了定義和儀器裝置中玻璃容器的材質(zhì)種類;規(guī)范了本標(biāo)準(zhǔn)中指示劑的描述,說明與藥典現(xiàn)行的甲基紅指示劑的區(qū)別;強(qiáng)調(diào)了本試驗(yàn)中試驗(yàn)用水的特殊要求,應(yīng)不含有重金屬,不含溶解性氣體。
4003<玻璃內(nèi)應(yīng)力測定法>完善了內(nèi)應(yīng)力概念,細(xì)化了檢測原理,明確了檢測目的,同時(shí)在測定法中區(qū)分為無色供試品和有色供試品的測定。
4006<內(nèi)表面耐水性測定法>明確了定義和測試原理,并在測定法中給出了灌裝體積的測定方法及精度要求,明確了滅菌器的升降溫及控溫精度要求。
4009<三氧化二硼測定法> 明確了原理和檢測目的,測定法中除采用鉑坩堝外,補(bǔ)充完善了鎳坩堝的使用方法,細(xì)化了操作,更利于檢驗(yàn)人員應(yīng)用。
3.2.2 阻隔性能相關(guān)測試方法
阻隔性能是影響產(chǎn)品在貨架期內(nèi)質(zhì)量的重要因素,也是確定貨架期的重要參考指標(biāo),通過檢測能避免藥品由于對氧氣或水蒸氣敏感而產(chǎn)生的氧化變質(zhì)、受潮霉變等問題。可用于控制包裝物的通透性、保障藥品在存儲(chǔ)期內(nèi)安全有效、指導(dǎo)選擇合適的包裝材料[2]。本版藥典收錄了4007<氣體透過量測定法>和4010<水蒸氣透過量測定法>兩個(gè)測定方法。
4007<氣體透過量測定法>保留兩項(xiàng)測定方法:第一法壓差法和第二法電量分析法。具體內(nèi)容按方法適用范圍、儀器裝置、測定法的順序進(jìn)行編寫。
4010<水蒸氣透過量測定法>主要收載三種測定方法:第一法重量法,根據(jù)原理進(jìn)行整合和梳理,按原理分為增重法和減重法,增重法中細(xì)分杯式法和容器法;第二法電解分析法;第三法紅外檢測器法。將具體內(nèi)容按方法名稱、測定原理、儀器裝置、測定法、附注的順序進(jìn)行編寫。
3.2.3 物理機(jī)械性能測試方法
物理機(jī)械性能是衡量藥品包裝在生產(chǎn)、運(yùn)輸、貨架期、使用等環(huán)節(jié)對內(nèi)容物實(shí)施保護(hù)的基礎(chǔ)指標(biāo),一般包括:拉伸強(qiáng)度與伸長率、熱合強(qiáng)度、剝離強(qiáng)度、熱收縮性、穿刺力、穿刺器保持性、插入點(diǎn)不滲透性、注藥點(diǎn)密封性、懸掛力等。本版藥典收載了4004<剝離強(qiáng)度測定法>、4005<拉伸性能測定法>、4008<熱合強(qiáng)度測定法>、4015<注射劑用膠塞、墊片穿刺力測定法>、4016<注射劑用膠塞、墊片穿刺落屑測定法>五個(gè)測定方法。
4004<剝離強(qiáng)度測定法>、4005<拉伸性能測定法>、4008<熱合強(qiáng)度測定法>均屬于材料的功能性指標(biāo)。方法均明確了定義和適用范圍,后續(xù)按儀器裝置、試驗(yàn)環(huán)境、試樣制備、測定法和結(jié)果判定闡述,由于材料的特性受環(huán)境的影響很大,在本處特別說明了樣品的放置條件和試驗(yàn)條件。
4015<注射劑用膠塞、墊片穿刺力測定法>和4016<注射劑用膠塞、墊片穿刺落屑測定法>均明確定義和適用范圍,為了更好地使用方法進(jìn)行檢測,將方法細(xì)分了三種,前兩種是針對膠塞,按應(yīng)用的注射劑裝量進(jìn)行區(qū)分,以50 mL為界;第三法是針對墊片。
3.2.4 生物安全性能測試方法
為加強(qiáng)藥包材的生物安全性評估,本版藥典收載了4011<藥包材急性全身毒性檢查法>、4013<藥包材溶血檢查法>和4014<藥包材細(xì)胞毒性檢查法>三個(gè)測定方法。
4011<藥包材急性全身毒性檢查法>從方法定義、試驗(yàn)用小鼠規(guī)定、供試品溶液和對照液制備、檢查法和結(jié)果判定方面對方法進(jìn)行了詳細(xì)的說明。如在供試品溶液制備中推薦了4種浸提條件,方便操作者選擇適宜的條件進(jìn)行試驗(yàn)。
4013<藥包材溶血檢查法>首先明確了定義,后續(xù)從試驗(yàn)前準(zhǔn)備(即新鮮抗凝兔血的制備)、供試品制備、檢查法和結(jié)果計(jì)算來描述。推薦了兩種常見的抗凝劑供操作者選擇。
4014<藥包材細(xì)胞毒性檢查法>收載了四種方法,即第一法相對增殖度法、第二法瓊脂擴(kuò)散法、第三法直接接觸法和第四法浸提法。分別從陰性、陽性對照液制備,檢查法和結(jié)果評價(jià)方面進(jìn)行闡述。其中細(xì)化了很多內(nèi)容,更有利于方法的選擇和使用,如推薦了供試品溶液制備的浸提比例和浸提條件、陽性對照制備中的生物毒性陽性參比物質(zhì)、明確了毒性分級劃分等內(nèi)容。
4 展望
我國醫(yī)藥產(chǎn)業(yè)已從滿足基本需求過渡到謀求高質(zhì)量發(fā)展階段。眾所周知“一流的企業(yè)做標(biāo)準(zhǔn)、二流的企業(yè)做品牌、三流的企業(yè)做產(chǎn)品”,而我國的藥用輔料和藥包材產(chǎn)業(yè)從產(chǎn)品的可及性、多元化、精細(xì)化、功能化、定制化等方面總體而言尚有較大的提升空間,參與國家標(biāo)準(zhǔn)、國際標(biāo)準(zhǔn)制定的硬實(shí)力和積極性均不夠高。《中國藥典》作為國家標(biāo)準(zhǔn)的法典,有義務(wù)、有意愿致力于強(qiáng)化“以標(biāo)準(zhǔn)促進(jìn)技術(shù)創(chuàng)新,以技術(shù)帶動(dòng)標(biāo)準(zhǔn)進(jìn)步”的共生效應(yīng)。
《中國藥典》2020年版的頒布不是終點(diǎn),而是新起點(diǎn),后續(xù)國家藥典委員會(huì)將繼續(xù)帶動(dòng)全行業(yè),共同加強(qiáng)藥用輔料和藥包材標(biāo)準(zhǔn)體系的不斷完善,助力我國藥品質(zhì)量與療效的提升,保障公眾用藥安全有效,以標(biāo)準(zhǔn)推動(dòng)國家治理現(xiàn)代化。(摘自《中國藥品標(biāo)準(zhǔn)》雜志)
《中國醫(yī)藥報(bào)》社版權(quán)所有,未經(jīng)許可不得轉(zhuǎn)載使用。
(責(zé)任編輯:李碩)
×
右鍵點(diǎn)擊另存二維碼!
網(wǎng)民評論
歡迎
登錄
-
為你推薦
-
熱點(diǎn)排行
- 2025年版《中國藥典》藥用輔料新增品種標(biāo)準(zhǔn)...
- 福建省藥監(jiān)局福州稽查辦監(jiān)督銷毀1.09余噸假...
- 藥監(jiān)“溫度”賦能產(chǎn)業(yè)“高度” 青海省醫(yī)...
- 吉林省藥監(jiān)局舉辦全省藥品流通監(jiān)管人員業(yè)務(wù)...
- 世界藥師日丨致敬你身邊的用藥守護(hù)者
- 巔峰對決展風(fēng)采藥物警戒護(hù)安全——2025年山...
- 每周醫(yī)藥看點(diǎn)(9月22日—28日)
- 湖北藥品網(wǎng)售新規(guī)10月起實(shí)施!監(jiān)管、平臺(tái)、...
- 湖南省藥監(jiān)局召開全省中藥飲片生產(chǎn)企業(yè)落實(shí)...
- 探索構(gòu)建罕見病診療與保障的“中國模式”
互聯(lián)網(wǎng)新聞信息服務(wù)許可證10120170033
網(wǎng)絡(luò)出版服務(wù)許可證(京)字082號
?京公網(wǎng)安備 11010802023089號 京ICP備17013160號-1













