新型藥物篩選研發平臺——SBDD
- 2020-08-12 09:36
- 作者:黃翰漾 孫媛媛 徐佳熹
- 來源:中國食品藥品網
隨著技術要求的不斷提升,在傳統新藥篩選技術的基礎上,一些新的藥物篩選平臺應運而生。本站將介紹五種新型藥物篩選研發平臺,本篇介紹第四種——SBDD。
什么是SBDD(基于結構的藥物發現平臺)
Structure-based drug design,即基于結構的藥物設計,從配體和靶點的三維結構出發,以分子識別為基礎而進行的一種藥物設計方法。根據藥物與其作用的靶點如受體、酶、離子通道、核酸、抗原、病毒等來尋找和設計合理的藥物分子。
通常SBDD的步驟包括:蛋白質結構制備、結合位點識別、配體庫制備、對接和評分功能。
靶點是藥物設計的先決條件,合理藥物靶點的選取直接決定了藥物開發的成敗。
靶點的三維結構,往往可以通過X-射線晶體學、多維核磁共振或同源蛋白質結構預測等計算機模型方法得到,其次利用實驗手段測定或用計算方法研究藥物與受體的作用模型,在此基礎上來進行合理藥物設計;除了考慮藥物與受體的結構特點,還需要考慮藥物的溶解性、毒性、代謝過程等因素的影響,合理藥物設計通常需要10-15次循環的努力才有可能找到“最為合適”的藥物分子。
SBDD技術平臺的優勢、不足
優勢:篩選成本低;可從少量化合物篩選獲得候選藥物;可顯著提高藥物發現命中率;可直接預測藥物-受體結合能。
不足:需要靶點完整清晰的三維立體結構;僅考慮藥物-受體的結合強度,不能預測藥物的藥效;速度慢。
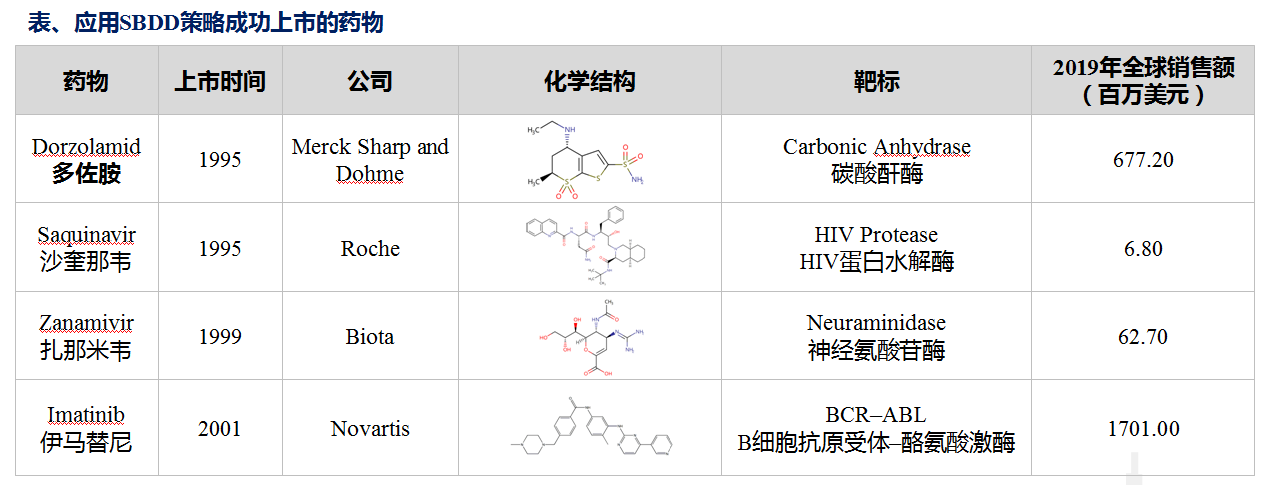
SBDD全球發展進程
其他在研藥品:Agouron 的AG85, AG337, AG331,靶標Thymidylate synthase(胸腺核酸合成酶);Roche在研產品,靶標Thrombin凝血酶,目前處于臨床Ⅱ期試驗階段。
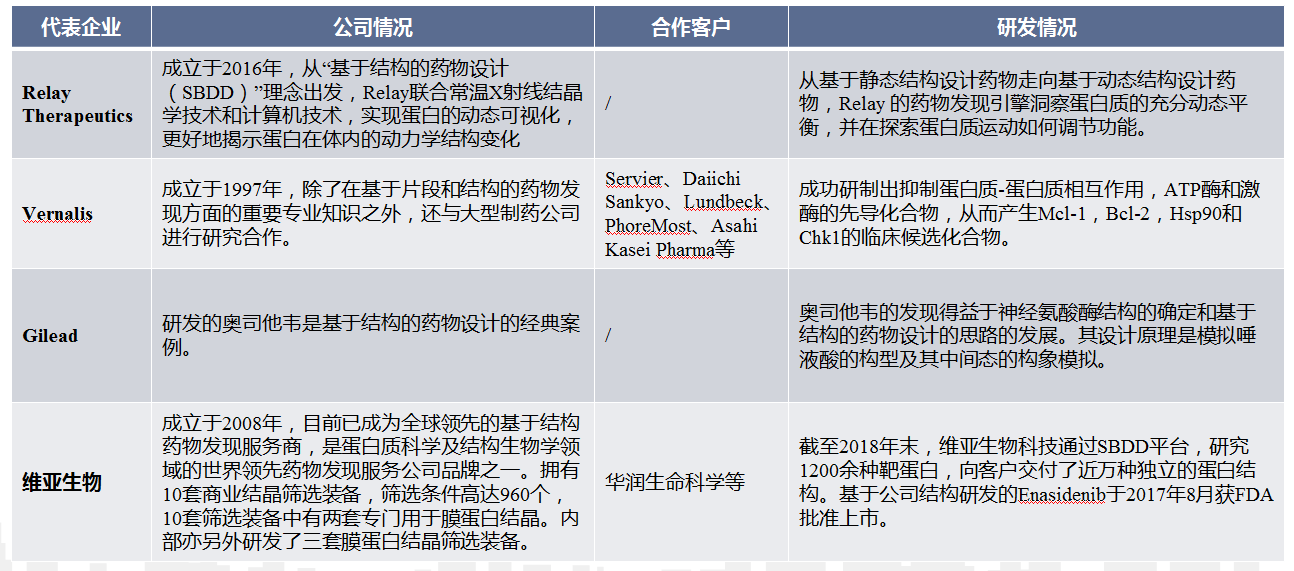
Relay Therapeutics:
成立于2016年,從“基于結構的藥物設計(SBDD)”理念出發,Relay聯合常溫X射線結晶學技術和計算機技術,實現蛋白的動態可視化,更好地揭示蛋白在體內的動力學結構變化。
從基于靜態結構設計藥物走向基于動態結構設計藥物,Relay的藥物發現引擎洞察蛋白質的充分動態平衡,并在探索蛋白質運動如何調節功能。
Vernalis:
公司成立于1997年,除了在基于片段和結構的藥物發現方面的重要專業知識之外,還與大型制藥公司進行研究合作。合作伙伴包括Servier、Daiichi Sankyo、Lundbeck、PhoreMost、Asahi Kasei Pharma等。
成功研制出抑制蛋白質-蛋白質相互作用,ATP酶和激酶的先導化合物,從而產生Mcl-1,Bcl-2,Hsp90和Chk1的臨床候選化合物。
Gilead:
Gilead公司研發的奧司他韋,從研究立項到成功上市只用了7年的時間,是基于結構的藥物設計的經典案例。奧司他韋的發現得益于神經氨酸酶結構的確定和基于結構的藥物設計的思路的發展。其設計原理是模擬唾液酸的構型及其中間態的構象模擬。
維亞生物:
成立于2008年,目前已成為全球領先的基于結構藥物發現服務商,是蛋白質科學及結構生物學領域的世界領先藥物發現服務公司品牌之一。
共有四種不同的蛋白質表達體系,包括大腸桿菌、酵母、昆蟲及哺乳動物細胞培養體系。
對于蛋白質表達,公司設計的結構體附有所有商業上可用的載體,并使用標簽,及在適當時進行蛋白質序列突變/插入/刪除。公司使用各種純化技術及蛋白質復疊技術,可制作穩定的同位素標記蛋白。
擁有10套商業結晶篩選裝備,篩選條件高達960個,10套篩選裝備中有兩套專門用于膜蛋白結晶。內部亦另外研發了三套膜蛋白結晶篩選裝備。
截至2018年末,維亞生物科技通過SBDD平臺,通過研究1200余種靶蛋白,向客戶交付了近萬種獨立的蛋白結構。
基于公司結構研發的恩西地平(Enasidenib),于2017年8月獲FDA批準用于具有IDH2基因特變患者的復發性或難治性急性髓性白血病(AML)。
相關鏈接:
風險提示:
1)新型藥物篩選技術發展存在不確定性;
2)新型藥物篩選研發平臺梳理尚不完善;
3)各研發平臺相關公司梳理尚不完善;
4)行業政策變化超預期。
本文僅代表作者觀點,不代表本站立場。
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:李碩)
右鍵點擊另存二維碼!
-
為你推薦













