siRNA藥物、適配體藥物、mRNA藥物……中國核酸制藥全景一覽
- 2020-07-24 15:44
- 作者:
- 來源:藥渡
核酸藥物是指具有治療疾病功能的DNA或者RNA,其能夠直接作用于致病靶基因或者靶mRNA,從根源上調控致病基因的表達,是精準醫療的有效手段之一。核酸藥物主要包括反義核酸、小干擾核酸、核酸適配體、小激活核酸、微小核酸、mRNA藥物、核酶等。
本文將就核酸制藥的中國業態情況進行系統梳理和分析。
核酸藥物分類及全球主要開發進展
反義核酸藥物
反義核酸藥物是發現最早、獲批最多的藥物,發展較成熟。自1978年Stephenson和Zammeenik首次在勞斯肉瘤病毒中發現反義寡核苷酸具有抑制病毒增殖的現象迄今,已經有7款藥物上市(如表1所示)。
表1 上市的ASO藥物
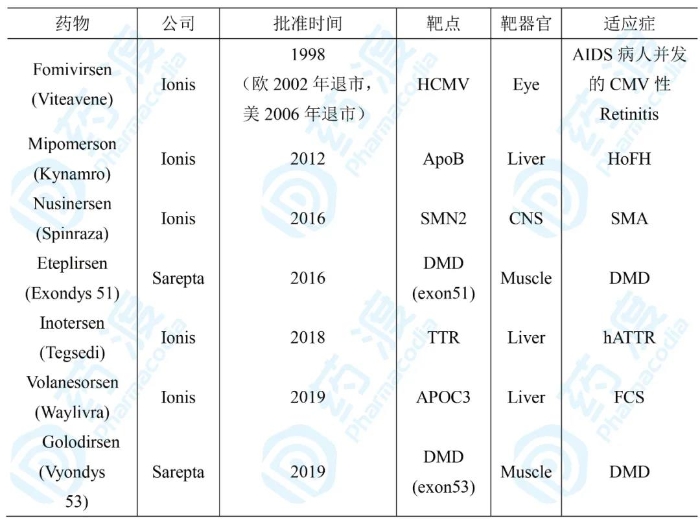
除兩款藥物由Sarepta開發外,其余五款均來自于反義核酸領域的領頭羊公司Ionis。該公司建立了一個高效且廣泛使用的藥物開發平臺,并基于該平臺與博健(Biogen)、羅氏(Roche)、阿斯利康(AstraZeneca)、諾華(Novartis)、楊森(Janssen)和葛蘭素史克(GSK)等多家跨國制藥公司建立了合作關系,目前有29種藥物進入臨床研究階段,覆蓋中樞神經系統疾病、罕見病、心血管代謝疾病、抗感染和腫瘤等領域,其中一款治療糖尿病的二期產品GCGR反義核酸的中國權益轉讓給了中國小核酸制藥領域領軍企業蘇州瑞博生物。
siRNA藥物
除反義核酸外,另一種轉錄后基因沉默機制是RNA干擾(RNAinterference, RNAi)。研究表明,將與mRNA對應的正義鏈和反義鏈組成的雙鏈RNA導入細胞,可以使mRNA發生特異性的降解,導致基因沉默,不表達相應的蛋白質。RNAi技術被《Science》雜志評為2001年的十大科學進展之一,卡內基研究所的AndrewFire和馬薩諸塞大學的Craig Mello因為發現RNAi機制而共享2006年的諾貝爾醫學或生理學獎。
2018年10月,全球第一款RNAi藥物PATISIRAN(商品名ONPATTRO?)獲得美國FDA批準上市,用于治療遺傳性甲狀腺素介導的淀粉樣變性的多發性神經病。該產品的上市,標志著RNAi療法應用的體內遞送問題得到了解決,證明了RNAi技術的臨床應用價值和商業開發價值。一年以后,Alnylam又宣布其旗下在研的RNAi療法新藥GIVLAARI(商品名GIVOSIRAN?)獲得美國FDA批準用于成年急性肝卟啉癥的治療。這是全球獲批的第二款RNAi療法藥物。跨國藥企又一次認識到RNAi技術的巨大潛力,和中小型平臺類公司合作開發siRNA藥物的案例再次出現(再生元/Alynlam、諾和諾德/Dicerna、強生/Arrowhead、BI/Dicerna等)。
目前全球已經有多款 siRNA 藥物處于臨床階段,在Onpattro和Givosiran之后,Quark/蘇州瑞博生物合作開發的視神經病變治療藥物QPI-1007及Quark在研藥物QPI-1002用于急性腎損傷適應證具有成為后續獲批上市品種的潛力。
saRNA藥物
具有基因激活功能的小dsRNA稱為小激活RNA(small activating RNA, saRNA)。與RNAi的沉默效果相比,RNAa的激活作用更為持久,它為腫瘤、代謝及遺傳性疾病的治療提供了一個嶄新的思路和方法。
RNA 激活現象(RNA activation,RNAa)最早由加州大學舊金山分校的李龍承博士和德克薩斯大學西南分校的 David Corey 在2006年發現。英國公司MiNA 獲得了二人專利的授權,于2016年發起了全球第一個運用 saRNAs 藥物MTL-CEBPA 對低響應率和高復發率的肝癌的臨床試驗。MTL-CEBPA項目的臨床前數據顯示,該化合物能促進幾種肝臟疾病模型的疾病進程逆轉,并減少肝癌的腫瘤負荷。目前MTL-CEBPA聯合索拉非尼治療肝癌的臨床試驗已經進展到臨床二期。
適配體藥物
2004年,美國FDA通過全球第一個用于治療AMD(老年濕性黃斑變性)的核酸適配體藥物Macugen。Macugen(哌加他尼鈉,Pegaptanib)是最早獲批用于眼科的抗VEGF類藥物。目前已上市的適配體藥物只有NeXstar公司研發的Macugen,2000年NeXstar公司將其轉讓給EyeTech,由OSI-Eytech和輝瑞公司共同研發和銷售,上市后Pfizer負責美國市場。但隨著2006年AMD治療領域迎來第二個抗VEGF藥物——雷珠單抗(Lucentis)獲批后,瞬間搶走Macugen市場,Macugen銷售額直線下降,2007年銷售額較2006年下降0.89億美元。2011年獲批的重組融合蛋白藥物阿柏西普(Eylea)雖然比Lucentis晚約5年上市,但短時間內就已經奠定了抗體(融合蛋白)在AMD領域的絕對優勢地位,2015年Eylea的銷售已經超過Lucentis。
表2 目前適配體藥物進展
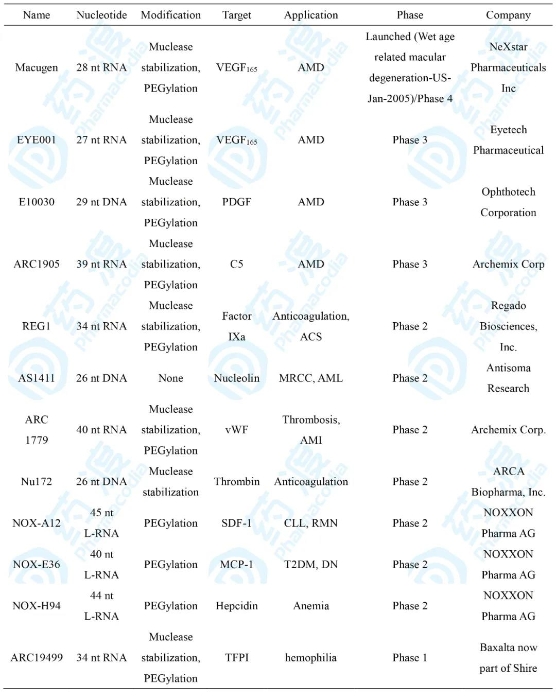
適配體(Aptamer)是一小段經體外篩選得到的寡核苷酸序列,其以獨特的空間結構與相應的配體進行高親和力和強特異性的結合,可以媲美抗體。與抗體相比,Aptamers具有以下理論上的特點:(1)Aptamers可以通過化學方法合成,獲得難度和成本更低;(2)Aptamers與抗體相比,免疫原性更低;(3)分子量小,組織穿透性好,易被細胞內化;(4)靶標更廣泛。據報道,Aptamers在腫瘤的免疫治療中具有重大潛力,可以降低腫瘤診斷和治療的成本。
mRNA藥物
據報道,僅在2015 年,和mRNA藥物研發相關的CureVac、Arcturus、BioNTech和 Moderna等公司累計獲得的融投資以及合作訂單金額超過40億美元。有人把這一年稱為mRNA藥物爆發的一年。
2016 年,隨著mRNA藥物和疫苗的臨床試驗進一步推進,投資者和醫藥巨頭繼續加碼。2016年9月,BioNTech公司宣布獲得羅氏集團旗下Genentech的3.1億美元投資,共同研發、生產基于mRNA的個性化癌癥疫苗。
mRNA作為藥物使用可指導細胞內蛋白質表達或者細胞外蛋白分泌。與用其他類型藥物治療疾病的方法有根本不同,mRNA療法既可以通過功能性蛋白的表達治療基因缺陷引發的疾病,又可以通過表達病毒或腫瘤抗原蛋白應用于疫苗,尤其在大規模突發性病毒感染以及腫瘤疫苗、個體化疫苗領域具有很好的潛力。
其他
核酶(Ribozyme)也是核酸藥物的一種,是一類具有生物催化活性的小分子RNA,可以特異性降解靶mRNA,從而阻斷特定基因的表達。核酶是1982年美國科學家T.Cech和他的同事在研究含有間隔內含子序列的rRNA前體時發現的,并因此獲得了1989年的諾貝爾化學獎。與其他RNA相比,核酶具有比較穩定的三維結構,不易受到RNA酶的攻擊。更重要的是,核酶在切斷mRNA后,又可以從雜交鏈上解脫下來,重新結合并切割其他的mRNA分子。這就意味著核酶在體內的活性很高,僅需少量即可發揮作用。核酶的種類很多,從結構上看,主要可以分為兩類,一類是發夾狀核酶,其切割活性需最小長度為50個核苷酸的片段,其中15個是必須的,這種結構的核酶通常由四個螺旋區和數個環裝區組成;另一類是錘頭狀核酶,長約30個核苷酸,有三個堿基配對的螺旋區、兩個單鏈區和一個膨出的核苷酸構成。隨著對核酶的研究不斷深入,人們已經認識到核酶在遺傳病、腫瘤和病毒性疾病上具有重大潛力。作為基因治療的一種方式,核酶已試用于HIV、HBV、HCV、HDV等;另外有些實驗使用核酶治療白血病在小鼠上已經取得了較好的效果。然而,基于某些不太明確的原因,到目前為止沒有任何核酶類藥物上市。
中國核酸技術/藥物代表公司
CRO類公司
上海吉凱基因
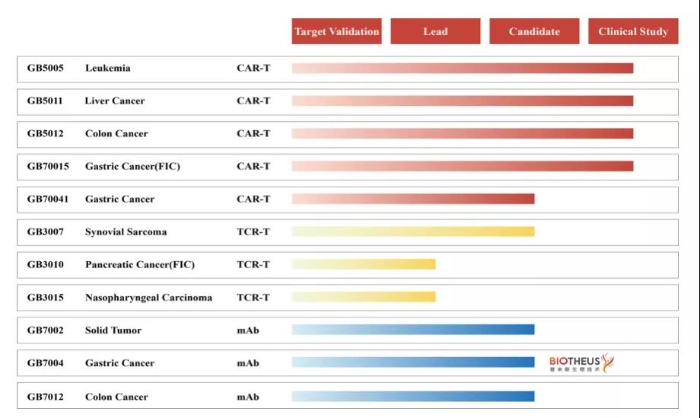
吉凱基因成立于2002年,是國內最早的RNAi服務提供商,提供RNAi產品生產和研發服務,包括RNAi產品、cDNA產品、microRNA產品、病毒產品、細胞產品及Cas9/TALEN等。吉凱基因在shRNA慢病毒包裝領域具有獨特的技術優勢,解決了難于轉染的組織、細胞的基因功能研究問題。近年來,吉凱基因也涉足醫藥領域,專注于細胞治療、基因治療和抗體藥物的開發,目前已建立有8個細胞治療產品和3個抗體產品的管線。
上海吉瑪
2003年,吉瑪基因在上海張江高科技園區創立,2007年在蘇州工業園區生物納米科技園設立總部,控股或參股多家子公司。目前公司有1.4萬平方米的生產研發場地,生產研發人員達300余人;具備了從RNA單體,RNA寡聚核酸分子合成,細胞組織高通量篩選,代謝組與基因組檢測,SPF動物/轉基因動物/PDX模型等多平臺組合,形成了完整的RNA研究解決方案。
另外,如蘇州貝信、蘇州鴻訊、天津賽爾、上海艾博思等公司通過不同的技術平臺在不同的核酸研究領域服務于不同層面的客戶。
反義核酸藥物公司——杭州天龍
2009年,杭州天龍藥業公司和浙江天龍創新藥物研究院成立,專業從事抗病毒與抗腫瘤兩大系列核酸新藥開發,核心產品包括CT102、Cantide與Flutide等系列核酸候選藥物,應用領域涵蓋流感、肝癌、手足口病、肝炎等國家重大疾病防治領域。其中CT102是具有自主知識產權的第一個反義核酸藥物,以IGF1R基因為靶點,擬用于治療肝細胞癌,于2018年3月取得臨床批件,目前處于臨床I期研究。帶頭人王升啟教授在核酸藥物研究領域有多年的積累,其帶領的團隊自1990年起在我國從零開始致力于反義核酸藥物研究,先后在國家自然科學基金、國家“863”計劃、國家重大新藥創制專項等資助下,攻克了該類藥物設計、規模化制備、質控等關鍵技術瓶頸。
siRNA藥物公司
蘇州瑞博
瑞博生物成立于2007年,致力于小核酸藥物研究和開發。自成立以來,該公司已經建立了專注于RNA干擾(RNAi)技術平臺、藥物發現及其他相關方面知識的專業化研發團隊,進而建立起一條豐富的小核酸藥物產品管線,適應證涵蓋感染、腫瘤、代謝、心腦血管和神經等多個疾病領域,包括針對乙型肝炎、高血脂癥等適應證的siRNA療法。目前該公司已有3個品種進入臨床試驗階段,其中2個產品進入全球臨床開發階段,另有多個品種即將申報IND。成立至今,瑞博開發出核酸制藥每個環節的關鍵技術,如siRNA候選序列的設計、活性篩選、核酸化學修飾、脫靶效應及免疫刺激反應評價、核酸化學以及生物分析方法、核酸制備工藝、中間體及藥品質量研究、核酸給藥技術及載體制備等,形成了較為完整的小核酸制藥技術鏈和藥物研發支撐體系,建立了包括核酸單體、原料藥、藥物遞送載體和藥物產品的工業生產能力,組建了核酸制藥專業的技術和管理團隊。
瑞博比較吸引眼球的是其與國外核酸藥物領軍企業進行的跨國合作。早在2012年,瑞博生物就與夸克制藥合作建立了合資公司RiboQuark(昆山瑞博夸克醫藥科技有限公司),并于2014年1月在中國提交了siRNA藥物QPI-1007的臨床試驗申請,這是一項治療非動脈炎性前部缺血性視神經病變的國際多中心2/3期關鍵性臨床試驗,于2015年獲批,已在中國完成首例受試者給藥。QPI-1007是一種人工合成的siRNA,旨在暫時抑制促凋亡蛋白半胱天冬酶2的表達。該研究是在中國進行的首個siRNA藥物的臨床試驗,該受試者也成為中國首例接受小核酸藥物治療的患者。其他適應證如青光眼的研究也在開展中。
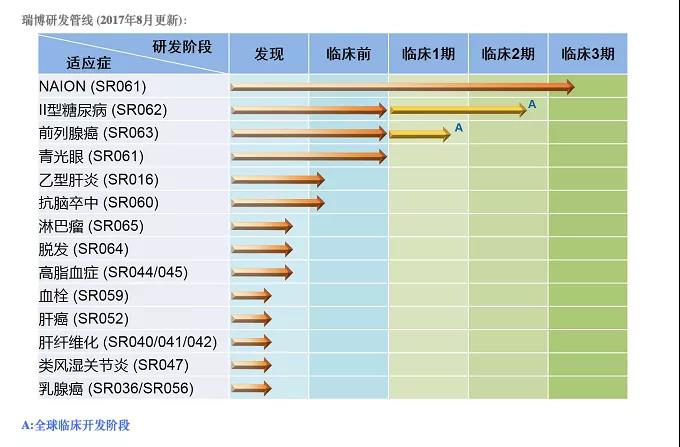
2013年,瑞博與美國Life Technologies Corporation就新一代小核酸遞送技術達成專利轉讓協議,瑞博獲得該技術在中國的研發和生產的獨占許可權利。Life Technologies曾是全球最大的生物技術企業(后被ThermoFisher公司收購),也是小核酸遞送技術領域的先行者,其體內、體外核酸遞送試劑占到國際小核酸轉染市場的70%。這是對瑞博的核酸藥物遞送技術平臺的一次有益補充,也為瑞博的諸多項目向臨床推進提供了非常好的支撐。
此外,瑞博生物通過與全球核酸制藥領先企業美國Ionis Pharmaceutical的合作,獲得了后者三個用于治療代謝疾病和癌癥的反義核酸藥物品種。
瑞博生物已經申請70余項專利,其中30余項獲得授權,涉及針對多種致病基因的siRNA及相關制劑、治療應用、給藥載體、核苷酸及寡聚核酸分子的工業化制備方法等。
2020年4月3日,瑞博獲得4.7億元人民幣的C2輪融資支持,截至此次融資,瑞博生物已獲超10億元融資支持。瑞博生物董事長梁子才博士表示,隨著兩個國際小核酸藥物的接連面市,小核酸制藥開始進入產業收獲期。瑞博生物也進入到快速發展階段。瑞博生物將不遺余力地繼續推進小核酸藥物品種研發和技術創新,爭取盡早為全球患者帶來更加精準、高效的治療手段。
蘇州圣諾
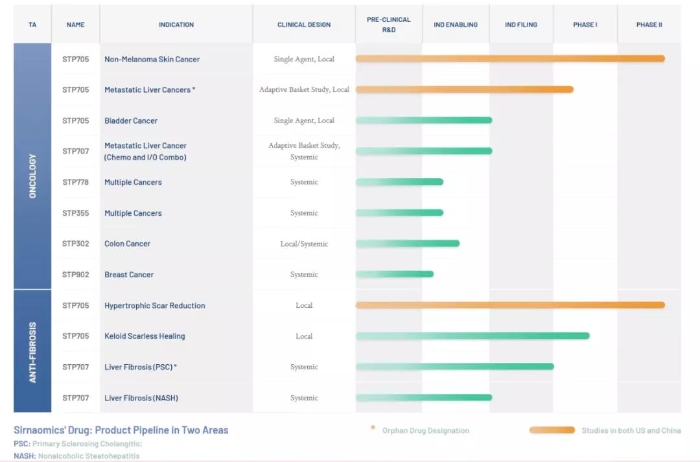
圣諾制藥(Sirnaomics)是一家專注于發現和開發針對癌癥和纖維化疾病RNAi療法的生物醫藥公司,總部位于美國馬里蘭州蓋瑟斯堡,子公司位于中國蘇州和廣州。該公司正致力于利用多能siRNA雞尾酒設計和納米粒子增強治療導入來推進其專有技術,用以治療疾病,治療領域包括抗纖維化藥物和癌癥治療藥物等。
圣諾制藥的領先候選產品STP705(科特拉尼注射劑)利用雙靶向抑制特性和多肽納米顆粒(PNP)優化載體系統,直接敲低TGF-β1和COX-2的基因表達。圣諾已獲得美國FDA和中國CFDA的多項臨床新藥研究(IND),包括非黑素瘤皮膚癌(NMSC)、膽管癌和增生性瘢痕的治療。根據圣諾產品管線,STP075治療非黑色素瘤皮膚癌項目已進行三期臨床試驗,目前試驗結果顯示STP075能夠殺死腫瘤細胞、縮小腫瘤。STP705還獲得了美國FDA授予的治療膽管癌和原發性硬化性膽管炎的孤兒藥資格,并指定該藥為治療肝細胞癌的孤兒藥候選藥物。這是該公司繼治療原發性硬化性膽管炎藥物和膽管癌藥物之后的第三個此類候選藥物。在一系列的臨床前研究中,STP705單藥被證實可顯著改善免疫T細胞在肝細胞癌(HCC)中的浸潤,同時也提高了PD-L1抗體在肝癌動物模型中的療效。這種效應除可作用于PD-1/PD-L1通路外,還可能會達到提高其他免疫檢查點抑制劑的療效。
saRNA藥物公司——中美瑞康
中美瑞康是一家初創型新藥研發企業,成立于2016年,公司致力于研發以“RNA激活”技術為核心的創新型藥與疾病治療方法。RNA激活(RNAa)技術是目前唯一能夠實現內源性基因激活并已進入臨床驗證的技術, 它通過重新開啟內源性基因的表達、恢復蛋白質的天然功能來治療疾病,有望填補現有靶向治療藥物只能抑制靶基因靶蛋白表達的巨大空白。中美瑞康正在開發針對多個疾病領域的候選藥物,尤其是罕見病領域,以解決高度未滿足的臨床需求。
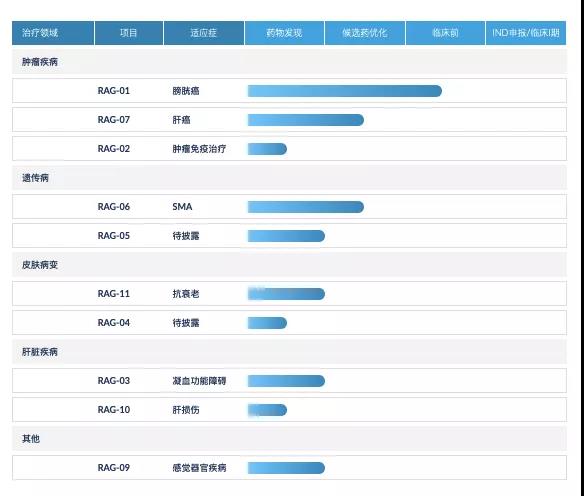
“RNA激活”(RNAactivation,簡稱RNAa)是一種新的生物學現象和基因調控機制,該機制能夠利用小分子RNA(也稱小激活RNA,saRNA)實現對體內基因的特異性和長效激活,是生命健康領域應用前景十分廣闊并已進入臨床驗證的前沿性技術,將為無數疾病包括很多目前尚缺乏治療方法的疾病帶來新的希望。
mRNA藥物公司
斯微生物
斯微生物成立于2016年5月,是一家致力于打造精準化癌癥免疫治療技術平臺,專注于mRNA癌癥個體化疫苗及miRNA靶向癌癥干細胞的藥物研發的高科技生物技術公司。斯微生物于2018年5月建成mRNA生產中心并開始產品管線研發,其第一個產品SM-Neo-Vac-1,是一款針對晚期消化系統腫瘤患者的新抗原個體化mRNA疫苗。
斯微生物于2019年7月完成了近億元的A輪融資,投資方包括張江火炬創投、隆門資本、久友智慧、伊泰久友和芳華投資,天使輪投資方龍磐投資追加投資。此輪融資將用于斯微生物mRNA 藥物GMP生產中心建設,并開展在三家醫院的臨床試驗及個性化腫瘤疫苗項目IND申報工作。斯微生物也將同步推進后續管線的前期研究。2020年2月,斯微生物又完成了由嘉興領峰股權投資合伙企業(有限合伙)和港股上市的君實生物共計3000萬元的A+輪融資。
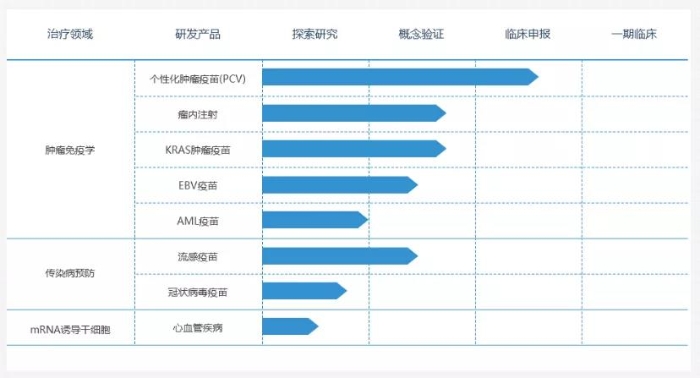
相對于其他核酸藥物,mRNA疫苗是通過在體外合成翻譯抗原的mRNA,然后遞送到體內由體內的細胞翻譯成抗原蛋白,無需在體外合成蛋白。所以相較于傳統疫苗長達數月的生產周期,mRNA疫苗僅需40天即可生產出來,具有獨特的時間優勢。但是,mRNA疫苗的研發技術門檻和要求也相對較高,對于新技術來說,安全性和有效性仍然是mRNA疫苗最大的挑戰。到目前為止,mRNA疫苗療法尚未完全取得臨床上的驗證,沒有任何一個正式的人用mRNA疫苗上市。
其他
復星醫藥與BioNTech達成合作,共同研發針對新冠病毒的疫苗產品。為了引進mRNA創新型技術,復星醫藥本次合作將斥資約1.35億美元。復星醫藥已經通過合作的方式進入核酸藥物領域。
核酸適配體藥物公司
2004年,美國FDA便通過第一個用于治療AMD的核酸適配體藥物Macugen,但目前國內沒有研究核酸適配體藥物的公司。因一次意外的發現,AS1411被作為適配體藥物研發至今,上世紀90年代末期,Bates的團隊設計出能形成三螺旋結構的核酸,檢測其對特定基因表達的調控作用。并設計一條由磷酸二酯鍵作為鏈接,只含有G和T剪輯的序列作為對照組,意外的是與靶基因毫無互補性的對照組卻顯示了更強的抗腫瘤活性。該團隊經后續的研究將其設計成含有26個堿基的序列,后被英國Antisoma公司購得,命名為AS1411。目前國內的湖南大學譚蔚泓團隊研發適配體藥物結合物(ApDC)AS1411雷公藤內脂醇結合物(ATC),為雷公藤甲素與核酸適配體偶聯,用于高效靶向治療三陰性乳腺癌。
microRNA藥物公司
昆山彭濟凱豐生物科技有限公司于2013年注冊成立,專注于研發微RNA(microRNA,miRNA)相關的小核酸新藥和微RNA生物試劑及技術服務,自建了微核酸藥庫并篩選到一批原創性的治療代謝類疾病和癌癥等方面的潛在微小分子核酸新藥,主要治療糖尿病、腎病。公司申報生物技術類、新藥發明專利18項,其中2項已獲授權,另外公司已遞交5項PCT申請。其中,可能填補市場空白的1.1類治療糖尿病腎病的小核酸新藥研發項目PJ150021于2018年獲得國家重大新藥創制科技重大專項立項支持。
CDMO公司
廣州銳博
銳博生物總部位于廣州開發區,擁有15年以上RNA合成與開發的豐富經驗,專注于核酸藥物(包括siRNA、反義核酸、miRNA、CRISPR及其他)的開發和生產,提供業界領先的一體化核酸藥物CDMO/CMO服務,包括寡核苷酸藥物設計、高通量合成與篩選、先導分子的發現與優化、靶向給藥系統開發、候選藥物的藥效研究、寡核苷酸藥物CMC服務(工藝開發、分析方法開發與驗證、穩定性研究和標準品研究)以及GMP生產等服務。
銳博是國內第一家做寡核酸藥物的CMO/ CDMO公司,并且也是國內首個獲得藥品生產許可證的GMP寡核酸生產基地。2017年,銳博與GE醫療簽署核酸藥物生產戰略合作協議,通過建立深度的戰略聯盟,共同推進國內核酸藥物的產業進展。
合全藥業
合全藥業是藥明康德的子公司,在中美兩地均有運營,服務于生命科學行業。作為全球新藥合作研究開發生產領域(CDMO)的領軍企業,合全藥業致力于為全球合作伙伴提供從臨床前到商業化,高效、靈活、高質量的一站式CMC(化學、生產和控制)解決方案。
2020年1月,合全藥業宣布,其寡核苷酸原料藥公斤級生產車間正式投入運營,該生產車間面積為2800平方米,坐落于合全藥業常州原料藥研發及生產一體化基地。目前,合全藥業的寡核苷酸平臺能夠支持各種類型的寡核苷酸產品,如脫氧核糖核酸(DNA),核糖核酸(RNA)和嗎啉代反義寡核苷酸(PMO)以及多肽共軛的嗎啉代反義寡核苷酸(PPMO)等。這標志著合全藥業能夠為全球客戶提供寡核苷酸原料藥從臨床前到商業化的一站式工藝開發及生產服務。
凱萊英醫藥集團
凱萊英醫藥集團作為全球領先的CDMO企業,已經在小分子藥物CMC領域深耕20余年,中西合璧的團隊以連續反應和生物轉化為代表的綠色制藥技術開發和應用,GMP和EHS管理體系的建立等,已經使凱萊英成為400多家包括全球Top10制藥公司和國內外生物醫藥研發公司的戰略合作伙伴或供應商。近年來,凱萊英在小分子CDMO領域取得的成功也逐步在以多肽和小核酸為代表的化學大分子和以抗體為代表的生物大分子CDMO業務中得到復制。
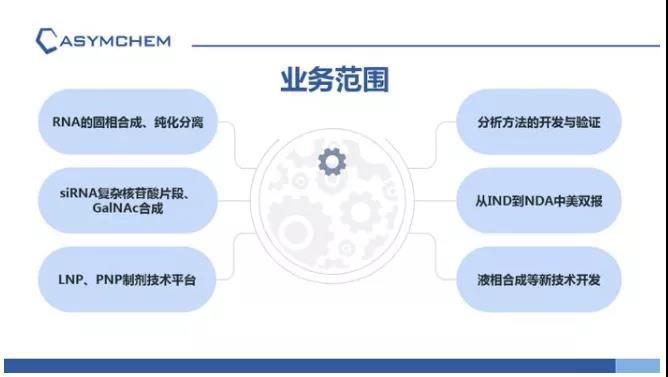
作為公司戰略發展的業務板塊,凱萊英積極投身于小核酸藥物的制藥技術研發,致力于為客戶搭建小核酸CMC一站式服務平臺。目前,凱萊英已經擁有超過50人涵蓋工藝開發、分析開發和GMP生產的小核酸團隊,設備投資接近1億元。目前,凱萊英已經為多個處于臨床前和臨床研究階段的小核酸藥物提供CMC服務。
小核酸給藥載體公司
杭州普施康
杭州普施康生物科技有限公司成立于2012年,是一家創新企業。專注于小分子藥物、核酸及多肽等藥物的新型納米藥物制劑的研發與產業化,主要應用于腫瘤、腦神經性疾病、血液疾病及肝硬化等方面的治療。公司旨在構建藥物納米傳遞的創新體系,協助醫藥企業進行產品升級和產品結構化調整,提升其企業競爭力,為大眾提供臨床療效更好的藥物。
納肽得
納肽得(青島)生物醫藥有限公司于2017年6月發起創立。公司定位于應用納米技術開發生物新藥,致力于國際領先的小核酸精準醫療產品研發,為癌癥治療提供靶向基因藥物和免疫藥物,同時研發高效低毒的多肽納米藥物傳遞系統,用于多種疾病的靶向治療。納肽得專注于尋找可以高效遞送siRNA的多種載體,最終實現利用小核酸技術治療疾病的目的。細胞外囊泡和自組裝納米粒技術是其核心技術平臺。
國內工業藥企在核酸藥物領域的大動作
綠葉生物2017年入股初創企業ExicureInc. 推進新型核酸藥物研發,領投1120萬美元私募融資,用于開發一種有望突破基因治療瓶頸的球形核酸療法(SNA)。
科倫藥業表示將會通過國際BD牽動前沿技術引進合作,包括核酸藥物,但目前尚未看到具體項目信息。
步長藥業全資子公司——丹紅藥業申請了2018年國家重大新藥創制項目,主要課題為重組新型蛋白藥物及基因治療,核酸藥物新品種研發及關鍵創新技術。
舒泰神致力于研發、生產和銷售臨床需求未被滿足的治療性藥物,包括基因治療/細胞治療藥物,其研發管線上的STSG-0002注射液,是治療乙型肝炎病毒感染相關疾病的基因藥物,從作用機制上,STSG-0002注射液為攜帶靶向HBV基因組P區和X區的shRNA序列表達框的肝噬性復制缺陷重組腺相關病毒。它以重組腺相關病毒(rAAV)作為遞送載體,將目的基因序列導入細胞轉錄生成shRNA,shRNA在細胞質中剪切為單鏈siRNA,隨后通過RNAi機制,特異性地沉默HBV復制相關的pgRNA和HBV蛋白表達相關的sRNA,阻斷HBV病毒復制,降低HBsAg、HBeAg和HBc蛋白的合成和分泌。還有治療艾滋病的小核酸基因藥物,但該項目尚處于保密階段,目前暫無可公開信息。
縱觀國內生物技術公司和制藥公司在核酸制藥領域的發展現狀,產業鏈基本完善:上游包括了核酸研究相關CRO,其中基因功能研究、核酸化學、核酸生物學等的研究結果為核酸藥物成藥及上市奠定堅實的基礎;中游包括藥物發現、給藥載體研究等,解決核酸制藥中的關鍵障礙;下游CDMO企業為產業化提供有力支撐。而制藥工業企業的介入,不僅提升了核酸制藥的信心,也為這個還在發展中的細分領域帶來制藥行業的基本經驗和資金支持,對于促進核酸藥物的快速發展具有積極作用。
做為平臺型的公司,核酸藥物公司的產品線很少集中于某個疾病領域。以中國第一家核酸制藥企業蘇州瑞博為例,其產品線涵蓋腫瘤、自身免疫性疾病、眼科、心腦血管、抗病毒、消化代謝等。這就是核酸藥物公司的優勢,不受疾病領域、靶點類型的限制,只要明確基因序列和基因與疾病之間的關系,就能開發出核酸藥物。
基因支持著生命的基本構造和性能,儲存著生命的孕育、生長、凋亡等過程的全部信息。核酸藥物作為能夠直接在基因水平影響病理過程的治療手段,與大自然的默契程度非常高。核酸藥物有望成為繼小分子化藥和單抗藥物之后的又一類爆款產品。(藥渡)
本文僅代表作者觀點,不代表本站立場。
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:李碩)
右鍵點擊另存二維碼!
-
為你推薦













