每周醫藥看點(5月27日—6月2日)
- 2024-06-04 13:59
- 作者:劉思慧
- 來源:中國食品藥品網
中國食品藥品網訊 市場監管總局就《市場監管部門優化營商環境重點舉措(2024年版)(征求意見稿)》公開征求意見;國家衛生健康委公示第五批鼓勵研發申報兒童藥品建議清單……5月27日—6月2日,醫藥行業的這些動態值得關注。
行業政策動態
1.市場監管總局就《市場監管部門優化營商環境重點舉措(2024年版)(征求意見稿)》公開征求意見。征求意見稿包括加快完善市場監管領域優化營商環境制度規則、推進嚴格規范公正文明執法、筑牢安全底線等10個部分,共計40條具體措施。其中,加快完善市場監管領域優化營商環境制度規則部分從市場準入、公平競爭、市場秩序、發展安全四個方面提出市場監管領域要重點完善的制度規則。征求意見稿提出,加快完善公平競爭制度規則,推動修訂《經營者反壟斷合規指南》,推動出臺《網絡反不正當競爭暫行規定》,研究制定《關于藥品領域的反壟斷指南》;加快完善市場秩序制度規則,修訂《市場監督管理嚴重違法失信名單管理辦法》,推動出臺《涉企違法違規收費行為處理辦法》等;加快完善“三品一特”制度規則,推動制修訂產品質量法、認證認可條例、藥品管理法實施條例、特種設備安全監察條例等法律法規,切實提高監管水平。
2.國家藥監局發布公告,氟馬西尼注射液、秋水仙堿片、甲氨蝶呤片、達沙替尼片、泊沙康唑腸溶片、泊沙康唑注射液、左乙拉西坦口服溶液7個藥品的說明書可以按要求增加兒童使用人群及用法用量。公告所附品種名單及藥品說明書修訂建議顯示,上述品種涉及兒童重大疾病(血液腫瘤、特發性關節炎)、兒童罕見病(家族性地中海熱)、兒童常見病多發病(癲癇)等治療領域。
3.國家衛生健康委公示第五批鼓勵研發申報兒童藥品建議清單。清單包括西替利嗪、阿托伐他汀等23個品種,涉及混懸劑、吸入溶液劑、口服溶液劑等多個劑型。
4.國家中醫藥管理局發布《中醫藥科技成果登記管理辦法(修訂)》,自公布之日起施行,2013年發布的《中醫藥科技成果登記辦法》同時廢止。辦法明確,中醫藥高等院校、科研院所、醫療機構應當登記,其他各類高等院校、科研院所、醫療機構以及相關企業自愿登記。每年初,由中醫藥科技成果登記機構組織登記上一年度通過評價(包括鑒定、驗收以及國家法律、法規規定的由專門機構進行審定)的中醫藥科技成果。
5.國家藥監局藥品審評中心(CDE)發布《在罕見疾病藥物臨床研發中應用去中心化臨床試驗的技術指導原則》。該指導原則結合罕見疾病特征,對罕見疾病藥物臨床研發過程中如何應用去中心化臨床試驗(DCT)提出建議,為罕見疾病藥物研發中科學、規范地開展DCT提供參考。該指導原則指出,無論是否采用DCT元素,均應遵循GCP的基本原則,即保護受試者的安全與權益,以及確保數據真實、可靠、可溯源。其中,保護受試者的安全與權益高于對其他因素的考量。在罕見疾病藥物臨床研發過程中應用DCT元素不應增加受試者的安全性風險。
6.CDE就《抗腫瘤藥物臨床試驗中SUSAR分析與處理技術指導原則(征求意見稿)》公開征求意見。指導原則旨在對抗腫瘤藥物臨床試驗進行試驗藥物安全性分析監測過程中,如何合理收集SUSAR,并進行科學分析,以協助發現、識別藥物安全性信號,從而助力于后續開展試驗藥物的安全風險評估,以及后續臨床研發和風險管理提供思路和建議。征求意見時限為自發布之日起一個月。
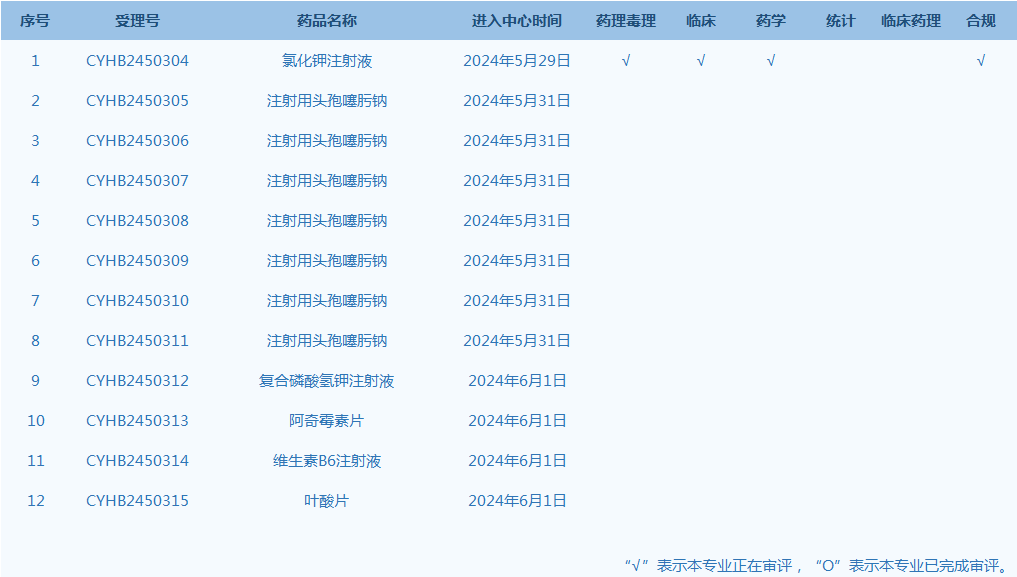
7.CDE網站公示12個仿制藥一致性評價任務,涉及氯化鉀注射液等品種(截至6月2日)。
產品研發上市信息
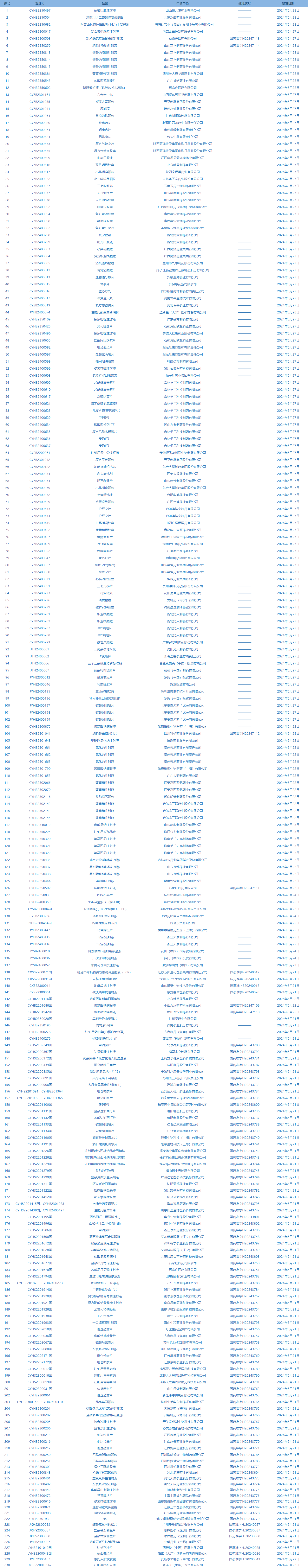
1.國家藥監局發布4期藥品批準證明文件送達信息,共包括230個受理號,涉及賽諾菲(中國)投資有限公司等企業(截至6月2日)。
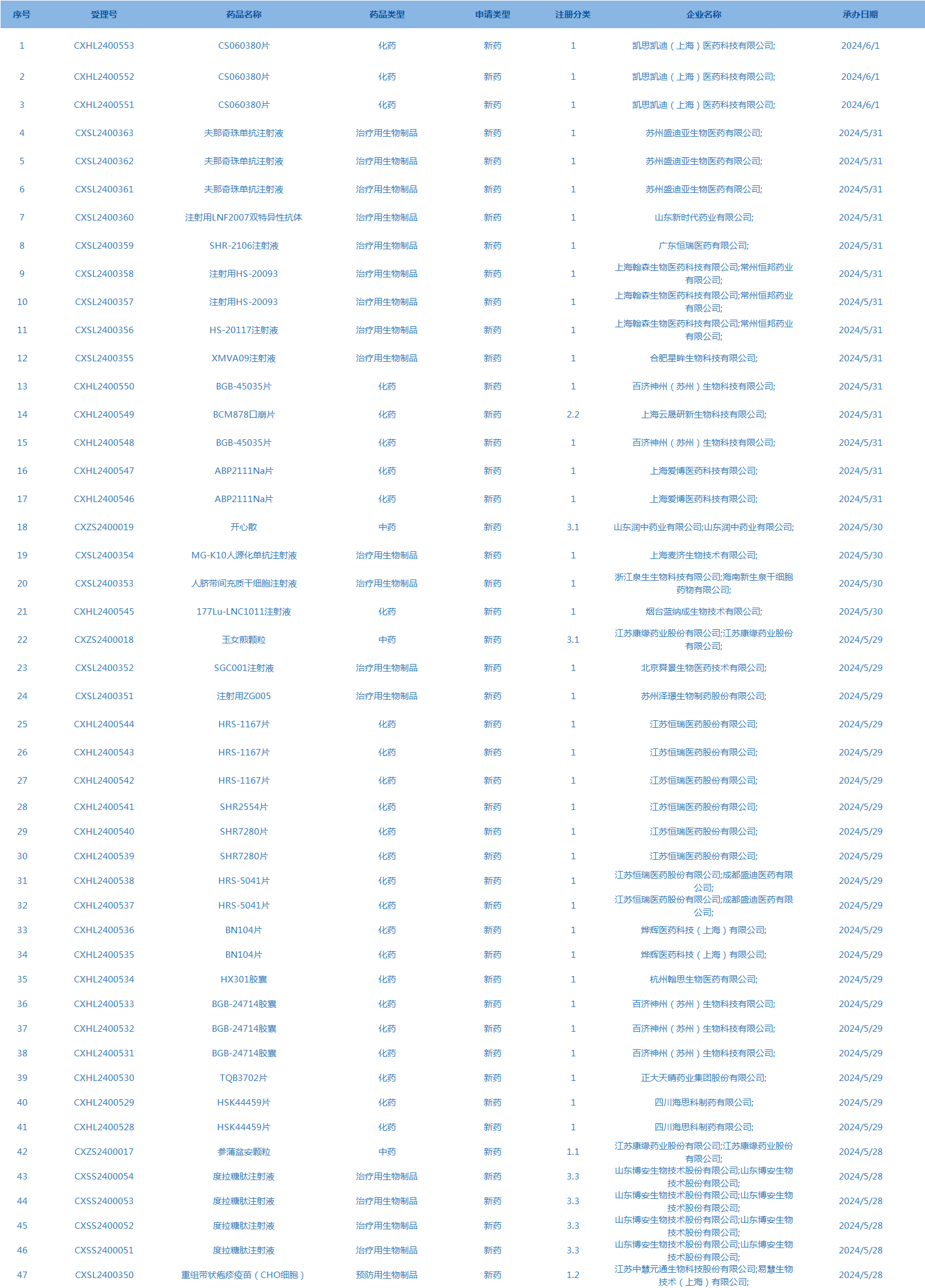
2.CDE承辦受理47個新藥上市申請,包括CS060380片等藥品(截至6月2日)。
3.輻聯科技宣布,其PSMA靶向放射性藥物225Ac-FL-020已獲得美國食品藥品管理局(FDA)新藥臨床試驗(IND)批準,用于治療轉移性去勢抵抗性前列腺癌(mCRPC)。
醫藥企業觀察
1.翰宇藥業發布公告稱,公司與三生蔓迪簽署《司美格魯肽注射液合作協議》。協議約定,公司將與三生蔓迪共同合作開發、獨家供應/采購、銷售分成司美格魯肽注射液(減重適應證)。三生蔓迪將向翰宇藥業支付里程碑付款、獨家采購價,以及約兩位數銷售提成。其中,里程碑付款主要由臨床前技術成果對價款、委托開發和注冊里程碑付款、條件性付款以及銷售里程碑付款四大部分組成。
2.輝大基因與美國Synthego公司共同宣布,雙方就高保真核酸酶hfCas12Max?達成許可合作。根據許可協議,輝大基因將授予Synthego擁有hfCas12Max?核酸酶生產和商業化銷售的權利,優化gRNA用于研究使用的權利,以及hfCas12Max?核酸酶用于治療目的的分許可權利。
3.百奧泰宣布與德國STADA公司就BAT2506(一款參照欣普尼開發的戈利木單抗生物類似藥)簽署授權許可及商業化協議。根據協議條款,百奧泰將負責BAT2506的研發、生產以及商業化供應,STADA將負責BAT2506在歐盟、英國、瑞士以及其他部分歐洲國家市場的商業化。在達到相應的里程碑事件后,百奧泰可獲得首付款加上里程碑款總金額最高至1.575億美元,以及凈銷售額的兩位數百分比作為收入分成。
藥品集中采購
1.河南省醫保局發布《關于做好國家組織胰島素接續集采等4個批次集中采購中選結果落地執行相關工作的通知》和《關于執行第八批國家組織藥品集中采購等6個批次中選結果第二采購周期有關事項的通知》,總共10個集采項目,共計1615個品規,涵蓋胰島素、短缺藥、干擾素、大容量輸液等品種,將于7月1日起執行。
2.江蘇省醫保局發布《關于開展第一二三批國家藥品集采接續采購續約工作的通知》。通知顯示,接續采購中選的過評產品愿意按不高于本產品全國省級及省際聯盟帶量采購最低中選(備選)價格、各省級現執行最低掛網價格和同品種國家集采平均中選價格(單片/粒/袋/支價格不超過0.1元的,以0.1元為準)三者中低值的價格繼續供應該省的,可繼續中選;未申報或申報價格不符合要求的,視為放棄中選身份。(劉思慧整理)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:劉思慧)
右鍵點擊另存二維碼!
-
相關閱讀
-
為你推薦













