2020盤點:FDA批準的53個新藥(二)
- 2020-12-29 11:04
- 作者:魏利軍
- 來源:中國食品藥品網
14.Pemazyre(pemigatinib)
4月17日,FDA加速批準了Incyte公司的成纖維生長因子(FGF)受體2抑制劑pemigatinib,用于攜帶FGFR2基因融合/重排、既往接受過治療且不可手術切除或局部晚期的膽管癌成人患者治療。膽管癌是一種非常罕見的癌癥,美國每年新確診患者約8000人,其中僅有15%的患者屬于FGFR2基因突變。EVP預測該產品在2026年的銷售額為3.35億美元。
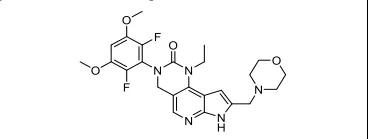
15.Trodelvy(sacituzumab govitecan-hziy)
4月22日,FDA加速批準了Immunomedics公司的抗體藥物偶聯物(ADC)sacituzumab govitecan,用于治療既往已接受至少2種療法的轉移性三陰性乳腺癌成人患者。轉移性三陰乳腺癌約占侵襲性乳腺癌的15%,目前治療手段仍以化療為主,但一般化療效果較差,應答率一般僅為10%-15%,PFS則只有2-3個月。Sacituzumab是一種靶向于TROP-2(人滋養層細胞表面抗原2)的人源化IgG1抗體,而govitecan是拓撲異構酶抑制劑伊立替康的代謝活性產物。除了三陰乳腺癌,本品開發的適應證還包括直腸癌、前列腺癌、胃癌等多種實體瘤,是2020年最值得關注的藥物之一。EVP預測該產品在2026年的銷售額可達21.51億美元。
16.Ongentys(opicapone)
4月24日,FDA批準了Neurocrine公司的新一代兒茶酚-氧位-甲基轉移酶(COMT)抑制劑opicapone,與甲基多巴和左旋多巴聯用,以改善帕金森病(PD)患者“關”時間。開關現象是PD患者長期應用左旋多巴出現的療效波動,而“關”主要表現為突然出現肢體僵直,運動不能,此前獲批用于改善開關現象治療的COMT抑制劑有托卡朋和恩他卡朋,但托卡朋因為肝毒性已經很少用。市場方面,本品早在2016年就獲得EMA批準上市,但市場表現平平。EVP預測該產品在2026年的銷售額為3.44億美元。
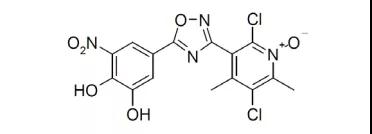
17.Tabrecta(capmatinib)
5月6日,FDA加速批準諾華公司的capmatinib上市,用于治療MET(上皮-間質細胞轉化)外顯子14跳躍突變的轉移性非小細胞肺癌(NSCLC)成人患者。攜帶MET外顯子14跳躍突變的NSCLC占肺癌患者總量的3%-4%,本品是首個獲FDA批準的針對性藥物。除了NSCLC,諾華還在開發乳腺癌、淋巴瘤和腎細胞癌等適應證。EVP預測該產品在2026年的銷售額可達3.55億美元。
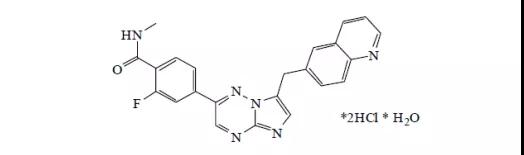
18.Retevmo(selpercatinib)
5月8日,FDA加速批準了Loxooncology公司的selpercatinib,用于治療RET(轉染重排基因)融合陽性的轉移性非小細胞肺癌和甲狀腺癌,以及RET基因突變的髓樣甲狀腺癌成人患者。Selpercatinib是首個獲得FDA批準用于RET基因改變的藥物。EVP預測本品在2026年的銷售額可達11.72億美元。
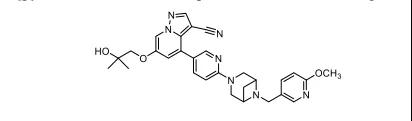
19.Qinlock(ripretinib)
5月15日,FDA批準Deciphera制藥的ripretinib上市,用于轉移性胃腸間質瘤四線治療。Ripretinib是一種廣譜KIT原癌基因受體酪氨酸激酶抑制劑和PDGFR(血小板衍生生長因子受體)α激酶抑制劑,基因檢測數據顯示,超過85%的胃腸間質瘤和系統性肥大細胞增多癥病例檢測到KIT或PDGFRA激酶,另外急性髓細胞白血病(AML)、黑色素瘤、生殖細胞腫瘤、肺癌和成膠質細胞瘤也存在一定比例的KIT或PDGFRA激酶,因此本品應用前景較廣,EVP預測本品在2026年的銷售額可達13.11億美元。
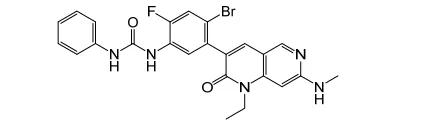
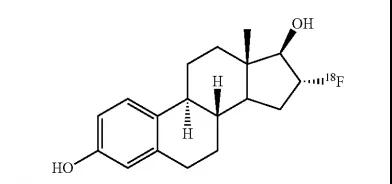
20.Cerianna(fluoroestradiol F18)
5月20日,FDA批準了Zionexa公司的含氟正電子發射型計算機斷層顯像(PET)劑,用于雌激素受體(ER)陽性病變檢測,作為復發或轉移性乳腺癌患者活檢的輔助手段。本品是一種F-18標記的F取代雌二醇,與雌激素受體有很強的親和力,而F-18是正電子放射性核素,可核變產生的正電子與周圍的負電子發生堙滅現象,產生湮沒輻射而成相。
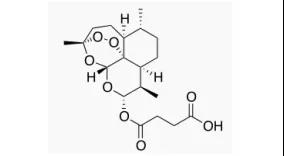
21.Artesunate(青蒿琥酯)
5月26日,FDA批準Amivas公司的青蒿琥酯用于成人或兒童嚴重瘧疾患者初始治療。瘧疾是對人類影響最大的傳染病之一,全世界有3億~5億人感染過瘧原蟲,每年有150萬~270萬人死于該病,其中90%以上病患在非洲。美國疾病控制與預防中心(CDC)數據顯示,美國每年僅有約2000個瘧疾確診病例,其中僅300例為重癥患者。
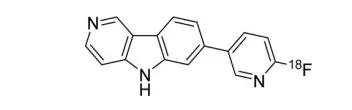
22.Tauvid(flortaucipir F18)
5月28日,FDA批準Avid Radiopharm的Tauvid上市,用于τ蛋白神經纖維糾結的密度和分布成像,為阿爾茨海默病(AD)診斷提供評估依據。Flortaucipir F18可與聚集的τ蛋白結合,靶向分布在病變區域。使用PET技術對病理性τ成像,將有助于AD早期診斷和疾病進展情況監測,在提倡AD疾病早期干預的時代背景下,τ蛋白和β-淀粉樣蛋白示蹤劑都具有巨大的發展潛力,是國外診斷巨頭們爭相布局的領域之一。
23.Uplizna(inebilizumab-cdon)
6月11日,FDA批準了Viela生物的inebilizumab,用于水通道蛋白4(AQP4)抗體陽性的視神經脊髓炎譜系疾病(NMOSD)治療。NMOSD是一種非常罕見的疾病,患者的免疫系統會錯誤地攻擊體內的健康細胞和蛋白質,大約50%的患者會發展成永久性視力障礙和癱瘓。流行病學數據顯示,約有1.6萬-1.7萬美國人罹患此病。除了NMOSD,本品還在開發腎移植、重癥肌無力等多種自免疫疾病。EVP預測該產品在2026年的銷售額可達5.18億美元。
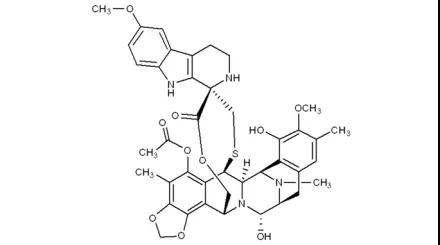
24.Zepzelca(lurbinectedin)
6月22日,FDA加速批準Jazz制藥的lurbinectedin上市,用于鉑類化療中進展或化療后進展的晚期小細胞肺癌(SCLC)治療。小細胞肺癌約占肺癌總數的13%-15%,目前治療仍以化療為主。市場潛力方面,EVP預測本品在2026年的銷售額可達3.97億美元。
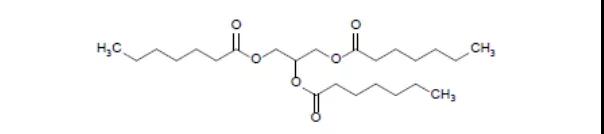
25.Dojolvi(三庚酸甘油酯)
6月30日,FDA批準了Ultragenyx公司的三庚酸甘油酯作為能量和脂肪酸的來源,用于長鏈脂肪酸氧化紊亂(LC-FAOD)患者治療。LC-FAOD是一種非常罕見且危及生命的常染色體隱性遺傳病,美國每年約有100名新生兒被確診為該病。該病患者因無法將長鏈脂肪酸轉化為能量而導致線粒體能量生成不足,臨床表現為心肌病、運動不耐受、頻繁肌痛,反復橫紋肌溶解和低血糖等。除了LC-FAOD,本品還在開展多項代謝失調的適應證研究。EVP預測其在2026年的銷售額為2.68億美元。(藥事縱橫 魏利軍)
本文的銷售額預測數據均來自Evaluate Pharma網站公開文章。本文已征得作者同意刊發,未經許可不得轉載。
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:劉思慧)
右鍵點擊另存二維碼!
-
為你推薦