華海:主動召回當點贊 權威回應解心憂
牙膏常用,但牙膏監管“不常見”,公眾對牙膏屬于化妝品的監管范疇還很陌生。同樣陌生的還有處方藥成分的氨甲環酸。功效牙膏的成分、宣傳等問題還需引起重視。
熱議程度:★★★☆☆
▍事件概述
2018年7月6日,華海藥業纈沙坦原料藥中檢測出亞硝基二甲胺(NDMA),引發輿論關注。隨后,華海藥業多次發布公告,說明事件進展及召回措施。期間,有自媒體傳播不實信息,引起網民恐慌。2018年7月29日,國家藥品監督管理局就該事件回應社會關切。2018年7月30日,國家衛生健康委員會發布通知,要求醫療機構做好配合召回和停止使用含華海藥業纈沙坦原料藥藥品的有關工作。
2018年9月28日,美國食品藥品管理局(FDA)、歐盟停止進口華海藥業生產的原料藥及制劑。2018年9月29日,華海藥業回應僅限川南生產基地。
2018年11月8日,諾華旗下山德士公司召回一批氯沙坦氫氯噻嗪片,因其原料藥中檢出N-亞硝基二乙胺(NDEA)雜質,原料藥為華海藥業生產。2018年11月10日、12日,華海藥業回應稱,原料藥雜質含量符合標準。
2018年12月11日,FDA公開了給華海藥業的警告信,引發部分自媒體質疑此前華海藥業公告與警告信內容不一致。2018年12月13日,華海藥業就此進行澄清。
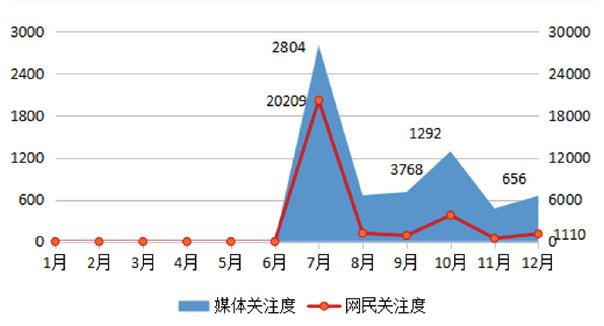
圖1 “云南白藥牙膏陷‘處方藥’風波”輿情走勢圖
▍輿情走勢
從整體輿情走勢看,如圖1所示,呈現“波浪式”特征,媒體關注度和網民關注度走勢一致。
第一階段:華海藥業原料藥中檢出NDMA,國家藥監局和國家衛健委相繼回應,輿情出現第一次高峰
2018年7月6日晚,華海藥業發布公告稱,纈沙坦原料藥中檢出致癌物NDMA。之后,華海藥業陸續發布4次公告,說明事件進展及召回措施。2018年7月22日,一些自媒體將事件與當時的“疫苗事件”相聯系,夸大事件的嚴重性和危害性。2018年7月23日,華海藥業發布澄清公告。全景網、界面新聞等進行轉載。2018年7月29日、30日,國家藥監局和國家衛健委分別就事件作出回應。新華網、中國新聞網等進行報道。
2018年8月初,潤都股份和天宇股份供應給臺灣客戶的纈沙坦原料藥中檢出NDMA成分。2018年8月10日、13日,兩家公司分別進行回應,界面新聞、第一財經等進行報道。
第二階段:FDA、歐盟禁止進口華海藥業原料藥及制劑,輿情出現第二次高峰
2018年9月28日,FDA、EMA發布禁令,停止進口所有華海藥業川南生產基地生產的原料藥及制劑產品。2018年9月29日,華海藥業發布情況說明稱,FDA的禁令僅針對川南生產基地,其他原料藥生產基地生產的產品不受禁令影響。2018年10月11日,微信公眾號“醫藥手機報”發文稱,FDA承認禁令只針對華海藥業川南廠區。財聯社、財經網、界面新聞等轉發相關信息。此后,EMA因在印度兩家藥企生產的其他沙坦類藥物中發現了NDEA雜質,將擴展審查范圍。
第三階段:山德士召回一批氯沙坦氫氯噻嗪片,輿情出現第三次高峰
2018年11月8日,諾華公司旗下山德士公司宣布在美國召回一批氯沙坦氫氯噻嗪片,因其原料藥中含有NDEA,該原料藥(氯沙坦鉀)由華海藥業生產。2018年11月10日、12日,華海藥業發布公告稱,山德士召回公告內容含糊,并未清晰完整地表述相關事實。公司原料藥NDEA含量符合歐盟、FDA及日本公布的標準。新京報網、中金在線等發布相關信息。
第四階段:FDA公開給華海藥業的警告信引質疑,華海藥業回應,輿情達到第四次高峰
2018年11月30日晚,華海藥業發布公告稱,收到FDA出具的警告信,針對重大不符合項進行匯總并提出整改要求。2018年12月11日,FDA警告信進行了公開。12日下午,雪球APP用戶“湯詩語”發文稱,纈沙坦雜質是客戶發現而非華海自查;華海藥業稱是使用了某種溶劑導致出現雜質,但FDA研究發現,不使用該溶劑也會出現雜質,華海公司并未找到原因;華海將客戶退回的原料藥處理之后賣給了非美國客戶。隨后,微信公眾號“賽柏藍”“GMP辦公室”等發文對警告信進行了翻譯,并與華海藥業公告進行了對比,相關信息助推輿情走高。2018年12月13日晚,華海藥業從NDMA雜質發現過程、如何處理問題批次、是否存在相關未知峰未做調查、NDMA雜質產生原因調查4個方面進行了澄清。
▍輿情點評
此次事件源于企業的主動信息披露。華海藥業的一系列公告、召回等行動也是在積極踐行企業的主體責任。從輿情走勢來看,華海藥業或權威部門的發聲是引起輿情波動的主要原因。同時,由于涉及藥品相關知識,專業性較強,網民關注度整體較低。僅在謠言出現、國家藥監局和國家衛健委發聲、歐盟擴展沙坦類藥物審查范圍等有煽動性、權威性和新鮮性的話題出現時,網民關注度才會大幅上升。
值得注意的是,在華海藥業披露信息不久,一些自媒體故意與當時的熱點事件相類比,傳播一些不實信息和夸張報道,惡意放大事件的危害性,激起了部分網民的恐慌情緒。信息的不對稱導致了公眾對用藥安全的擔心。因此,在類似專業性要求很強的事件中,在普通公眾并不能十分理解個中道理的情況下,需要從他們關心的實際切身問題出發,及時給出明確的信息、實用的指導、有效的解決辦法,才能更好的安撫公眾情緒。
在事件發展過程中,不斷有新的話題拋出,而且相關問題波及到了國內外更多的企業和產品。事件也逐步從一個由國內企業引發、國內外同步召回的用藥安全事件上升到行業問題。
鑒于此,我國的藥品監管部門應督促相關藥企采取必要措施進行自查和整改,加強針對性的抽檢,并在全國范圍內加強對沙坦類藥物的風險排查,防范風險。同時,加深對原料藥生產工藝與檢測技術的探討,組織專家進行風險評估。此外,事件一定程度上對華海藥業國內和國際市場造成影響,甚至使中國原料藥在國際市場的形象下降,給中國藥企在國際市場的競爭造成負面沖擊。除了企業積極回應外,是否需要組織專家給予專業的解讀,也是值得監管部門思考的問題。