2020年專利保護到期 多家企業瞄準他達拉非市場蛋糕
隨著全球人口老齡化及工作壓力的增大,勃起功能障礙(ED)患者數量呈現逐年增長趨勢。世界衛生組織(WHO)發布的數據顯示,全球男性ED患者約占全球男性總人數的10%。到2025年,全球ED患者人數將達到3.2億人。
在我國,ED發病率也呈上升趨勢。在一項對北京、重慶、廣州三個城市ED發病率進行的調查中,2226名20歲以上男性調查問卷結果顯示,40歲以上的男性ED患病率為40.2%;另一項針對40歲以上男性進行的調查問卷結果也顯示,約有四成40歲以上的男性患有ED。
輝瑞原研藥西地那非是抗ED藥物領域的開山鼻祖。但目前在全球抗ED藥物市場,禮來公司的他達拉非已成為銷售冠軍。他達拉非在我國的專利保護2020年到期,目前已有多家企業提交仿制藥申請,但還沒有企業拿到批文。
我國暫無他達拉非仿制藥獲批
2002年11月,他達拉非首先在歐洲上市,用于ED的治療;2003年2月,他達拉非分別在英國、瑞典、丹麥、德國及澳大利亞等多個國家上市,適應證均為用于ED的治療;2003年11月,他達拉非在美國上市。至此,他達拉非完成了在歐美等國際主流市場的上市,且適應證均為ED治療。
2009年7月,他達拉非在美國增加了新的適應證——PAH(肺動脈高壓)的治療;2011年10月,FDA批準他達拉非另一種適應證——BPH(良性前列腺增生)的治療。
2014年4月,他達拉非在日本推出,用于治療BPH及其引起的尿失禁。
他達拉非為口服薄膜衣片,在全球上市的規格為2.5mg、5mg、10mg、20mg。我國也已經進口,各規格都已經陸續推出。需要注意的是,根據他達拉非美國藥品說明書中的用法用量,可根據個體差異將實際使用劑量降到2.5mg、5mg,這種小規格的產品在臨床上有細分市場價值。
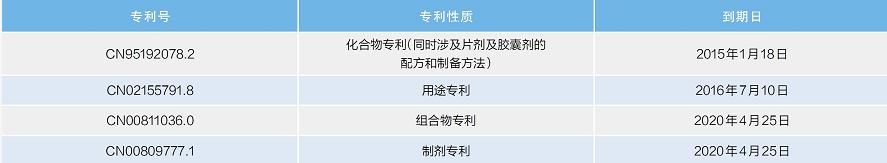
表1 他達拉非在我國的核心專利
他達拉非原研企業——禮來公司對其申請的專利共有11件,在我國獲得4項核心專利(見表1)。這4項專利構成了他達拉非在我國的核心保護壁壘。
目前國內已經有38家企業申請他達拉非片仿制,其中不乏南京正大天晴制藥有限公司、江蘇恒瑞醫藥股份有限公司這樣的大企業。但由于各種原因,至今還沒有一家企業拿到仿制藥生產批文。華潤賽科藥業有限責任公司于2015年10月最早拿到了他達拉非片的臨床批件;另有3家企業申請了他達拉非口溶膜劑的改劑型申報;正大天晴于2014年申請了他達拉非咀嚼片的改劑型申請,并獲得臨床批件。在38家企業中,共有35家申請了他達拉非生物等效性試驗,目前21家已經完成。
他達拉非仿制藥市場前景廣闊
禮來原研藥他達拉非,起初在全球市場的銷售表現平平, 2006年銷售額僅為2億美元左右;但從2007年開始,該產品銷售額快速增長,當年銷售額達11.44億美元,一舉成為重磅炸彈級別藥物;之后每年銷售額都處于增長狀態,2012年,他達拉非銷售額達21.51億美元,2017年達23.23億美元。
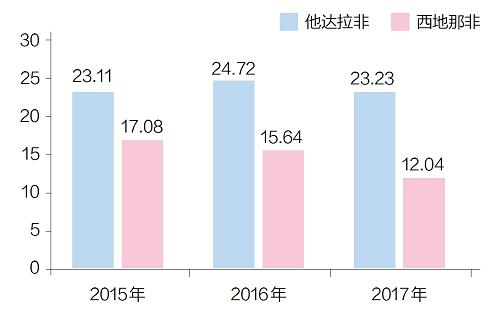
圖1 2014~2017年他達拉非樣本醫院銷售數據(萬元)
據中國藥學會的數據,2017年,他達拉非在我國樣本醫院的銷售額為3600萬元左右(見圖1),且銷售額保持穩步增長。在我國,他達拉非主要銷售途徑為醫院和零售藥店,其中零售藥店銷售額占比約84.7%。
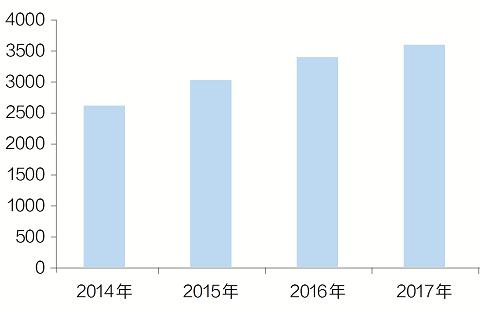
圖2 2015~2017年他達拉非與西地那非全球銷售數據(億美元)
縱觀全球銷售數據,他達拉非早已取代西地那非,成為全球ED市場銷售冠軍,兩者具體銷售數據見圖2。而在我國,處在ED市場銷售額第一的還是西地那非,2017年全國醫院及零售終端銷售額為22.3億元,而他達拉非僅為7.4億元。
他達拉非在國際與國內市場表現不一,與西地那非更早進入我國密不可分,西地那非“藍色小藥片”的形象更容易讓患者接受。但由于他達拉非對PDE5的抑制性高于西地那非,半衰期大于17h(西地那非為4h),藥效可維持24h~36h的臨床治療優勢,未來,他達拉非在我國將會受到更多關注。此外,通過國際市場銷售數據也可以看出,未來他達拉非在我國市場前景可期。
他達拉非在我國的專利保護期到2020年。我國仿制藥一旦獲批上市,勢必會對進口原研藥形成沖擊,再加上藥品帶量采購政策的推出,他達拉非仿制藥在我國會更具競爭力。[劉志寧 作者單位:華諾通(北京)醫藥科技有限公司]